Zellulärer Lipidstoffwechsel
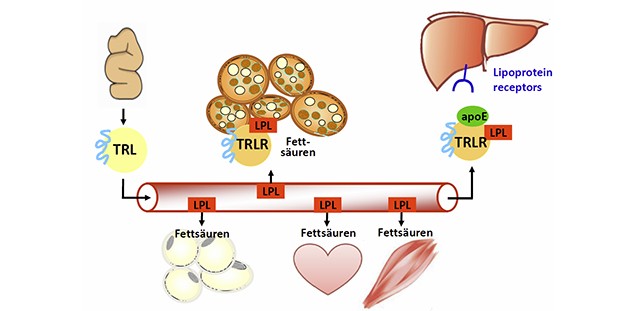
Fette (Lipide) aus der Nahrung werden in der wässrigen Umgebung des Blutes in Lipoproteinen transportiert. Der postprandiale Lipoprotein-Stoffwechsel beschreibt den Transport von Fetten im Blut, die Aufnahme von Lipiden ins Fettgewebe und in die Leber sowie den weiteren intrazellulären Stoffwechsel der aufgenommenen Lipoproteine nach der Nahrungsaufnahme. Die medizinische Relevanz dieser Thematik ergibt sich aus der Tatsache, dass die Entstehung der Atherosklerose und die daraus resultierende koronare Herzkrankheit aber auch Insulinresistenz und Diabetes mellitus Typ II maßgeblich mit Abnormalitäten im postprandialen Lipoprotein-Stoffwechsel assoziiert sind.
Projekte
Der Forschungsschwerpunkt der Arbeitsgruppe ist es, die Regulierung und Bedeutung der durch Lipide ausgelösten pathophysiologischen Prozesse zu verstehen, die zu Übergewichts-bedingten chronischen Stoffwechselerkrankungen wie Typ-2-Diabetes und Herz-Kreislauf-Erkrankungen führen. Zu diesem Zweck untersuchen wir die organspezifische Regulierung des Lipid-Stoffwechsels unter physiologischen Bedingungen und wollen verstehen, wie veränderte Stoffwechselflüsse von Lipiden zwischen Fettgewebedepots und der Leber die Entstehung von Stoffwechselkrankheiten fördern. Ein besonderer Schwerpunkt liegt auf dem braunen Fettgewebe, einem spezialisierten Organ, das bei Menschen, Nagetieren und anderen Säugetieren vorkommt und über einen als adaptive Thermogenese bekannten Prozess Wärme erzeugen kann. In den letzten Jahren haben wir einen umfassenden Überblick über die systemische und parakrine Regulierung des intravaskulären Triazylglyzerid- und Cholesterinstoffwechsels sowie des intrazellulären Lipidhandlings unter Bedingungen thermogener Aktivierung gegeben, die einen tiefgreifenden Einfluss auf entzündliche Signalwege im Fettgewebe, Arterien und in der Leber haben. So konnten wir die Relevanz des braunen Fettgewebes für den systemischen Fett- und Lipoproteinstoffwechsel aufzeigen, und neue physiologische und pharmakologische Mechanismen entschlüsseln, die über die Aktivierung des braunen Fettgewebes die Behandlung von Übergewichts-bedingten kardiometabolischen Stoffwechselerkrankungen ermöglichen könnten.
Projekt 1. Purinerge Rezeptoren bei Entzündungen im Fettgewebe und adaptiver Thermogenese
Adipositas ist durch einen gestörten Energiestoffwechsel im weißen und braunen Fettgewebe gekennzeichnet. Die assoziierten metabolischen Veränderungen lösen Entzündungsreaktionen aus und tragen damit wesentlich zur Entwicklung chronisch entzündlicher Stoffwechselkrankheiten wie Typ-2-Diabetes bei. In diesem Projekt wollen wir die funktionelle Bedeutung extrazellulärer Adenin-Nukleotide und purinerger Rezeptoren für die Lipidprozessierung, die adipogene Differenzierung und für Entzündungsreaktionen im weißen und braunen Fettgewebe untersuchen.
Projekt 2. Intestinale Metaboliten und ihr Einfluss auf thermogene Reaktionen in braunem und weißem Fettgewebe
Mikrobielle Metabolite wie kurzkettige Fettsäuren und Gallensäuren können thermogene Reaktionen im braunen und weißen Fettgewebe modulieren. Die Konzentration der intestinalen Metaboliten im systemischen Kreislauf wird durch die Gatekeeper-Funktion der Leber bestimmt, welche dadurch den Energieverbrauch in braunen und beigen Adipozyten kontrolliert. Die Relevanz dieses Organ-Crosstalks für die adaptive Thermogenese und den systemischen Energiestoffwechsel soll im Zusammenhang mit einem humanisierten Gallensäurepool und T-Zell-vermittelter Entzündung in der Leber untersucht werden.
Projekt 3. Bedeutung der endothelialen Lipoproteinverarbeitung für die Plastizität und Funktion des thermogenen Fettgewebes
Zum Auffüllen der Energiespeicher als Reaktion auf die kälteinduzierte Thermogenese internalisieren braune und beige Adipozyten große Mengen an Fettsäuren, die von Triglyzerid-reichen Lipoproteinen (TRL) geliefert werden. Zusätzlich werden ganze TRL-Partikel durch vaskuläre Endothelzellen (ECs) von aktiviertem braunem Fett internalisiert. Wir wollen den Mechanismus der Partikelaufnahme sowie die intrazelluläre Verarbeitung von TRL-Lipiden durch ECs entschlüsseln. Die Relevanz dieser Prozesse soll im Zusammenhang mit der adaptiven Thermogenese und dem systemischen Energiestoffwechsel untersucht werden.
Projekt 4. Regulierung des Energiestoffwechsels im braunen Fett durch Lipidaufnahme und Lipidverarbeitung in Makrophagen des Fettgewebes
Fettgewebsmakrophagen (ATM) sind zusammen mit Fettzellen ein wesentlicher Bestandteil des Fettgewebes. Hier nehmen sie neben ihrer klassischen Immunfunktion auch Lipide auf und verarbeiten sie und tragen so zum Fettstoffwechsel bei. Ihre funktionelle Bedeutung für den thermogenen Fettstoffwechsel ist jedoch nur unzureichend bekannt. In diesem Projekt wollen wir die Rolle der ATM-Lipidaufnahme und -verarbeitung während der Aktivierung des thermogenen Fettes entschlüsseln. Insbesondere werden wir die Immun- und Stoffwechselfunktion von ATM sowie die Auswirkungen von ATM auf die thermogene Funktion von Adipozyten und auf den systemischen Energiestoffwechsel untersuchen.
Projekt 5. Die Rolle der ChREBP-abhängigen de novo Lipogenese für die metabolischen und thermogenen Aktivitäten des braunen und weißen Fettgewebes
Braune und beige Adipozyten weisen eine hohe de novo Lipogenese (DNL), die Synthese endogener Fettsäuren, auf. Die Gründe für die hohe DNL-Kapazität in thermogenen Fettgeweben sind unbekannt. Wir haben herausgefunden, dass das carbohydrate response element-binding protein (ChREBP) die DNL-Enzyme in braunen Adipozyten kontrolliert. In diesem Projekt wollen wir untersuchen, wie ChREBP-Isoformen die DNL und andere zelluläre Funktionen im thermogenen Fettgewebe regulieren. Außerdem wollen wir Mechanismen identifizieren, die DNL mit der adaptiven Thermogenese verbinden.
Projekt 6. Einfluss von Kälte-induziertem Energieumsatz auf den Knochenumbau
Eine enge Verbindung von Knochen-Remodellierung und Energiestoffwechsel wird durch zahlreiche Studien mit genetisch modifizierten Mausmodellen, aber auch durch klinische Beobachtungen, unterstützt. So ist Fettleibigkeit in der Regel mit erhöhter Knochenmineraldichte assoziiert, während niedriges Körpergewicht als Risikofaktor für osteoporotische Frakturen gilt. Darüber hinaus entstehen Adipozyten und Knochen-bildende Osteoblasten aus den gleichen Vorläuferzellen, und verminderte Osteoblasten-Differenzierung tritt bei osteoporotischen Patienten oft in Verbindung mit Verfettung des Knochenmarks auf. In diesem Projekt wird die Interaktion zwischen Energiestoffwechsel und Knochen-Remodelling untersucht, wobei das Kälte-induzierte Molekül identifiziert werden soll, welches die Knochenbildung hemmt. Die Blockade eines solchen Moleküls oder seines Rezeptors wäre ein attraktiver Ansatz zur osteoanabolen Behandlung von Knochenmasseverlust-Syndromen.
Projekt 7. Interaktionen zwischen Stoffwechsel und Entzündungsprozessen: Molekulare und zelluläre Signale in Organen und Organoiden
Die Manifestation chronisch-entzündlicher Erkrankungen wird durch genetische und exogene Faktoren bestimmt. Unbestritten ist, dass ein Überangebot von hochkalorischer Nahrung und Übergewicht zu einem gestörten metabolischen Gleichgewicht führen. Diese Veränderungen bewirken in Stoffwechsel-aktiven Organen entzündliche Reaktionen in den Zellen des angeborenen und adaptiven Immunsystems. Das Ziel dieses interdisziplinären Verbundprojektes ist es, molekulare und zelluläre Interaktionen zwischen Stoffwechsel, Immunologie und Entzündung im Darm, Fettgewebe und Leber zu erfassen, um die pathophysiologischen Prozesse chronischer Volkskrankheiten wie Diabetes, Nicht-alkoholischer Leber und Darm-Entzündung und Colitis mechanistisch aufzuklären. Zu diesem Zweck soll das komplexe Zusammenspiel zwischen Ernährung, Metaboliten und Immunzellen mit modernsten Laser-gestützten Multi-Omics- und Imaging-Technologien in Organen und Organoiden systembiologisch untersucht werden.
Kooperationen der Arbeitsgruppe Lipidstoffwechsel
- Ein DAAD Projekt zum wissenschaftlichen Austausch wird bis Ende 2009 finanziert. Projektpartner ist Prof. Dr. Carlos Enrich aus Barcelona, Spanien.
- Ein DFG-Antrag (Merkel / Heeren) mit dem Titel: Apolipoprotein A5: Funktion im Fettstoffwechsel und Bedeutung bei der Entstehung der Arteriosklerose ist im November 2007 bewilligt worden.
- Das Projekt "Regulation des endosomalen LRP1-Transportes" wird im Rahmen des von der DFG neu eingerichteten Graduiertenkollegs "Sortierung und Wechselwirkung zwischen Proteinen subzellulärer Kompartimente" (Sprecher Prof. Thomas Braulke) untersucht.
Nationale Kooperation
- PD Dr. med. Andreas Niemeier, Zentrum für Operative Medizin, UKE
- Dr. med. Martin Merkel, Asklepios Klinik St. Georg
- Dr. rer. nat. Johannes Herkel, Zentrum für Innere Medizin, UKE
- Prof. Dr. med. Franz Rinninger, Zentrum für Innere Medizin, UKE
- Prof. Dr. Paul Saftig, Institut für Biochemie, Universität Kiel
Internationale Kooperationen
- Dr. Thomas Grewal, University of New South Wales, Sydney, Australien
- Prof. Carlos Enrich, Universität Barcelona, Spain
- Prof. Gunilla Olivecrona, Universität Umea, Schweden
- Prof. Philippa Talmud, Royal free and University College Medical School London, Great Britain
Publikationen
Cold exposure reduces trabecular and cortical bone mass in wildtype and Dio2-deficient mice
Behler-Janbeck F, Baranowsky A, Stenzel P, Neven M, Yorgan T, Amling M, Worthmann A, Heeren J, Schinke T
ENDOCRINOLOGY. 2026;167(3):.
Shiny-Calorie: a context-aware application for indirect calorimetry data analysis and visualization using R
Grein S, Elschner T, Kardinal R, Bruder J, Strohmeyer A, Gunasekaran K, Witt J, Hermannsdóttir H, Behrens J, U-Din M, Yu J, Heldmaier G, Schreiber R, Rozman J, Heine M, Scheja L, Worthmann A, Heeren J, Wachten D, Wilhelm-Jüngling K, Pfeifer A, Hasenauer J, Klingenspor M
BIOINFORM ADV. 2026;6(1):vbaf270.
Infrared laser sampling of low volumes combined with shotgun lipidomics reveals lipid markers in palatine tonsil carcinoma
Kerkhoff L, Moritz M, Eggert D, Worthmann A, Heeren J, Zech H, Clauditz T, Wilczak W, Schlüter H, Betz C, Böttcher A, Hahn J
MOL ONCOL. 2026.
A GDF-15-GFRAL axis controls autoimmune T cell responses during neuroinflammation
Sonner J, Kahn A, Binkle-Ladisch L, Engler J, Haack B, Zeiler C, Unger L, Bauer S, Fischbach F, Almanzar G, Walkenhorst M, Mayer C, Kolakowska A, Graute S, Ramien C, Winschel I, Rothammer N, Heine M, Horneffer-van der Sluis V, Thiemann V, Vieira V, Meurs N, Renné T, Prelog M, Jørgensen S, Seeley R, Diemert A, Arck P, Gold S, Heeren J, Wischhusen J, Friese M
NAT IMMUNOL. 2026;27(3):503-515.
Maternal lipids in overweight and obesity: implications for pregnancy outcomes and offspring's body composition
Albrecht M, Worthmann A, Heeren J, Diemert A, Arck P
SEMIN IMMUNOPATHOL. 2025;47(1):1-21.
Single-nucleus mRNA-sequencing reveals dynamics of lipogenic and thermogenic adipocyte populations in murine brown adipose tissue in response to cold exposure
Behrens J, Wang T, Kilian C, Worthmann A, Herman M, Heeren J, Adlung L, Scheja L
MOL METAB. 2025;101:102252.
Effects of time-of-day on the noradrenaline, adrenaline, cortisol and blood lipidome response to an ice bath
Braunsperger A, Bauer M, Brahim C, Seep L, Tischer D, Peitzsch M, Hasenauer J, Figueroa S, Worthmann A, Heeren J, Dyar K, Koehler K, Soriano-Arroquia A, Schönfelder M, Wackerhage H
SCI REP-UK. 2025;15(1):1263.
Endothelial SR-B1 is dispensable for thermogenesis but promotes selective cholesterol uptake in brown adipose tissue
Hurkmans K, Heine M, Rinninger F, Jaeckstein M, Mineo C, Shaul P, Heeren J
J LIPID RES. 2025;66(10):100894.
Purinergic adipocyte-macrophage crosstalk promotes degeneration of thermogenic brown adipose tissue
Jaeckstein M, Fischer A, Rissiek B, Staehler T, Heine M, Behrens J, Mann O, Pfeifer A, Magnus T, Schlein C, Worthmann A, Scheja L, Koch-Nolte F, Heeren J
EMBO REP. 2025;26(24):6460-6493.
The Purinergic Receptor P2X5 Modulates Glucose Metabolism and Expression of Thermogenic Genes in Brown Adipose Tissue
Jaeckstein M, Miegel L, Behrens J, Stähler T, Diercks B, Heine M, Koch-Nolte F, Heeren J
INT J MOL SCI. 2025;26(13):.
Diet modulates the therapeutic effects of dimethyl fumarate mediated by the immunometabolic neutrophil receptor HCAR2
Kosinska J, Assmann J, Inderhees J, Müller-Fielitz H, Händler K, Geisler S, Künstner A, Busch H, Worthmann A, Heeren J, Sadik C, Gunzer M, Prévot V, Nogueiras R, Hirose M, Spielmann M, Offermanns S, Wettschureck N, Schwaninger M
ELIFE. 2025;14:e98970.
Fructose uptake by brown adipose tissue is independent of carbohydrate response element-binding protein and does not cause elevated de novo lipogenesis
Scheja L, Behrens J, Heine M, Jaeckstein M, Fuh M, Heeren J, Siebels B, Worthmann A, Haas D, Krahmer N
ACTA BIOCH BIOPH SIN. 2025 [Epub ahead of print];57(x):1-14.
Sex differences in lipidomic and bile acid plasma profiles in patients with and without coronary artery disease
Bay B, Fuh M, Rohde J, Worthmann A, Goßling A, Arnold N, Koester L, Lorenz T, Blaum C, Kirchhof P, Blankenberg S, Seiffert M, Brunner F, Waldeyer C, Heeren J
LIPIDS HEALTH DIS. 2024;23(1):197.
The short-chain fatty acid receptors Gpr41/43 regulate bone mass by promoting adipogenic differentiation of mesenchymal stem cells
Behler-Janbeck F, Baranowsky A, Yorgan T, Jaeckstein M, Worthmann A, Fuh M, Gunasekaran K, Tiegs G, Amling M, Schinke T, Heeren J
FRONT ENDOCRINOL. 2024;15:1392418.
An efficient AAV vector system of Rec2 serotype for intravenous injection to study metabolism in brown adipocytes in vivo
Behrens J, Braren I, Jaeckstein M, Lilie L, Heine M, Sass F, Sommer J, Silbert-Wagner D, Fuh M, Worthmann A, Straub L, Moustafa T, Heeren J, Scheja L
MOL METAB. 2024;88:.
The TRPM2 ion channel regulates metabolic and thermogenic adaptations in adipose tissue of cold-exposed mice
Benzi A, Heine M, Spinelli S, Salis A, Worthmann A, Diercks B, Astigiano C, Pérez Mato R, Memushaj A, Sturla L, Vellone V, Damonte G, Jaeckstein M, Koch-Nolte F, Mittrücker H, Guse A, De Flora A, Heeren J, Bruzzone S
FRONT ENDOCRINOL. 2024;14:1251351.
Time-resolved role of P2X4 and P2X7 during CD8+ T cell activation
Brock V, Lory N, Möckl F, Birus M, Stähler T, Woelk L, Jaeckstein M, Heeren J, Koch-Nolte F, Rissiek B, Mittrücker H, Guse A, Werner R, Diercks B
FRONT IMMUNOL. 2024;15:1258119.
Multimodal image-guided laser ablation system for precise 3D tissue sampling and subsequent analysis of biomolecules for cancer research
Hahn J, Moritz M, Walter A, Wieck T, Moustafa A, Mansour W, Harms C, Stenzel P, Heeren J, Haider M, Lange T, Schlüter H
2024. Imaging, Manipulation, and Analysis of Biomolecules, Cells, and Tissues XXII. Tárnok A, Houston J (Hrsg.). 1. Aufl. Bellingham, Washington: SPIE , .
CD73-dependent generation of extracellular adenosine by vascular endothelial cells modulates de novo lipogenesis in adipose tissue
Jaeckstein M, Schulze I, Zajac M, Heine M, Mann O, Pfeifer A, Heeren J
FRONT IMMUNOL. 2024;14:1308456.
Unlocking the paracrine crosstalk: adipocyte-derived factors affect carbonic anhydrase IX expression in colon and breast cancer cells
Lapinova J, Balaz M, Balazova L, Csaderova L, Golias T, Zatovicova M, Heeren J, Pastorekova S, Takacova M
NEOPLASMA. 2024;71(2):164-179.
Mitochondrial dysfunction abrogates dietary lipid processing in enterocytes
Moschandrea C, Kondylis V, Evangelakos I, Herholz M, Schneider F, Schmidt C, Yang M, Ehret S, Heine M, Jaeckstein M, Szczepanowska K, Schwarzer R, Baumann L, Bock T, Nikitopoulou E, Brodesser S, Krüger M, Frezza C, Heeren J, Trifunovic A, Pasparakis M
NATURE. 2024;625(7994):385-392.
The triglyceride-synthesizing enzyme diacylglycerol acyltransferase 2 modulates the formation of the hepatitis C virus replication organelle
Reichert I, Lee J, Weber L, Fuh M, Schlaeger L, Rößler S, Kinast V, Schlienkamp S, Conradi J, Vondran F, Pfaender S, Scaturro P, Steinmann E, Bartenschlager R, Pietschmann T, Heeren J, Lauber C, Vieyres G
PLOS PATHOG. 2024;20(9):.
EPAC1 enhances brown fat growth and beige adipogenesis
Reverte-Salisa L, Siddig S, Hildebrand S, Yao X, Zurkovic J, Jaeckstein M, Heeren J, Lezoualc'h F, Krahmer N, Pfeifer A
NAT CELL BIOL. 2024;26(1):113-123.
Fatty acid synthesis suppresses dietary polyunsaturated fatty acid use
Worthmann A, Ridder J, Piel S, Evangelakos I, Musfeldt M, Voß H, O'Farrell M, Fischer A, Adak S, Sundd M, Siffeti H, Haumann F, Kloth K, Bierhals T, Heine M, Pertzborn P, Pauly M, Scholz J, Kundu S, Fuh M, Neu A, Tödter K, Hempel M, Knippschild U, Semenkovich C, Schlüter H, Heeren J, Scheja L, Kubisch C, Schlein C
NAT COMMUN. 2024;15(1):45.
Acute Deletion of the Glucocorticoid Receptor in Hepatocytes Disrupts Postprandial Lipid Metabolism in Male Mice
Correia C, Præstholm S, Havelund J, Pedersen F, Siersbæk M, Ebbesen M, Gerhart-Hines Z, Heeren J, Brewer J, Larsen S, Blagoev B, Færgeman N, Grøntved L
ENDOCRINOLOGY. 2023;164(10):.
Live-cell imaging identifies cAMP microdomains regulating β-adrenoceptor-subtype-specific lipolytic responses in human white adipocytes
De Jong K, Ehret S, Heeren J, Nikolaev V
CELL REP. 2023;42(5):112433.
TREM2 Regulates the Removal of Apoptotic Cells and Inflammatory Processes during the Progression of NAFLD
Liebold I, Meyer S, Heine M, Kuhl A, Witt J, Eissing L, Fischer A, Koop A, Kluwe J, Wiesch J, Wehmeyer M, Knippschild U, Scheja L, Heeren J, Bosurgi L, Worthmann A
CELLS-BASEL. 2023;12(3):.
The lysosomal LAMTOR / Ragulator complex is essential for nutrient homeostasis in brown adipose tissue
Liebscher G, Vujic N, Schreiber R, Heine M, Krebiehl C, Duta-Mare M, Lamberti G, de Smet C, Hess M, Eichmann T, Hölzl S, Scheja L, Heeren J, Kratky D, Huber L
MOL METAB. 2023;71:101705.
Short-term dietary changes can result in mucosal and systemic immune depression
Siracusa F, Schaltenberg N, Kumar Y, Lesker T, Steglich B, Liwinski T, Cortesi F, Frommann L, Diercks B, Bönisch F, Fischer A, Scognamiglio P, Pauly M, Casar C, Cohen Y, Pelczar P, Agalioti T, Delfs F, Worthmann A, Wahib R, Jagemann B, Mittrücker H, Kretz O, Guse A, Izbicki J, Lassen K, Strowig T, Schweizer M, Villablanca E, Elinav E, Huber S, Heeren J, Gagliani N
NAT IMMUNOL. 2023;24(9):1473-1486.
Lipidome Analysis of Oropharyngeal Tumor Tissues Using Nanosecond Infrared Laser (NIRL) Tissue Sampling and Subsequent Mass Spectrometry
Stadlhofer R, Moritz M, Fuh M, Heeren J, Zech H, Clauditz T, Schlüter H, Betz C, Eggert D, Böttcher A, Hahn J
INT J MOL SCI. 2023;24(9):.
Loss of hepatic SMLR1 causes hepatosteatosis and protects against atherosclerosis due to decreased hepatic VLDL secretion
van Zwol W, Rimbert A, Wolters J, Smit M, Bloks V, Kloosterhuis N, Huijkman N, Koster M, Tharehalli U, de Neck S, Bournez C, Fuh M, Kuipers J, Rajan S, de Bruin A, Ginsberg H, van Westen G, Hussain M, Scheja L, Heeren J, Zimmerman P, van de Sluis B, Kuivenhoven J
HEPATOLOGY. 2023;78(5):1418-1432.
Role of Liver CD38 in the Regulation of Metabolic Pathways during Cold-Induced Thermogenesis in Mice
Benzi A, Spinelli S, Sturla L, Heine M, Fischer A, Koch-Nolte F, Mittrücker H, Guse A, De Flora A, Heeren J, Bruzzone S
CELLS-BASEL. 2022;11(23):.
Susceptibility to diet-induced obesity at thermoneutral conditions is independent of UCP1
Dieckmann S, Strohmeyer A, Willershäuser M, Maurer S, Wurst W, Marschall S, de Angelis M, Kühn R, Worthmann A, Fuh M, Heeren J, Köhler N, Pauling J, Klingenspor M
AM J PHYSIOL-ENDOC M. 2022;322(2):E85-E100.
Lysosomal acid lipase promotes endothelial proliferation in cold-activated adipose tissue
Fischer A, Jaeckstein M, Heeren J
ADIPOCYTE. 2022;11(1):28-33.
Metabolic Turnover Studies to Quantify Energy Uptake by Thermogenic Adipose Tissues of Mice
Heine M, Corban C, Heeren J
2022. Brown Adipose Tissue. 1. Aufl. New York, NY: HUMANA PRESS INC, 107-118.
Apoptotic brown adipocytes enhance energy expenditure via extracellular inosine
Niemann B, Haufs-Brusberg S, Puetz L, feickert m, Jaeckstein M, Hoffmann A, Zurkovic J, Heine M, Trautmann E, Müller C, Tönies A, Schlein C, Jafari A, Eltzsching H, Gnad T, Blüher M, Krahmer N, Kovacs P, Heeren J, Pfeifer A
NATURE. 2022;609(7926):361–368.
A Gas Chromatography Mass Spectrometry-Based Method for the Quantification of Short Chain Fatty Acids
Rohde J, Fuh M, Evangelakos I, Pauly M, Schaltenberg N, Siracusa F, Gagliani N, Tödter K, Heeren J, Worthmann A
METABOLITES. 2022;12(2):.
Novel Adipose Tissue Targets to Prevent and Treat Atherosclerosis
Scheja L, Heeren J
2022. Prevention and Treatment of Atherosclerosis. von Eckardstein A, Binder C (Hrsg.). 1. Aufl. Cham: Springer, 289-310.
Pregnancy-induced maternal microchimerism shapes neurodevelopment and behavior in mice
Schepanski S, Chini M, Sternemann V, Urbschat C, Thiele K, Sun T, Zhao Y, Poburski M, Woestemeier A, Thieme M, Zazara D, Alawi M, Fischer N, Heeren J, Vladimirov N, Woehler A, Puelles V, Bonn S, Gagliani N, Hanganu-Opatz I, Arck P
NAT COMMUN. 2022;13(1):.
Increased concentrations of conjugated bile acids are associated with osteoporosis in PSC patients
Stürznickel J, Behler-Janbeck F, Baranowsky A, Schmidt T, Schwinge D, John C, Lohse A, Schramm C, Heeren J, Schinke T, Amling M
SCI REP-UK. 2022;12(1):.
Role of Endothelial Cell Lipoprotein Lipase for Brown Adipose Tissue Lipid and Glucose Handling
Thiemann E, Schwaerzer G, Evangelakos I, Fuh M, Jaeckstein M, Behrens J, Nilsson S, Kumari M, Scheja L, Pfeifer A, Heeren J, Heine M
FRONT PHYSIOL. 2022;13:.
Replication of SARS-CoV-2 in adipose tissue determines organ and systemic lipid metabolism in hamsters and humans
Zickler M, Stanelle-Bertram S, Ehret S, Heinrich F, Lange P, Schaumburg B, Kouassi N, Beck S, Jaeckstein M, Mann O, Krasemann S, Schroeder M, Jarczak D, Nierhaus A, Kluge S, Peschka M, Schlüter H, Renné T, Pueschel K, Kloetgen A, Scheja L, Ondruschka B, Heeren J, Gabriel G
CELL METAB. 2022;34(1):1-2.
Role of CD38 in Adipose Tissue: Tuning Coenzyme Availability?
Benzi A, Grozio A, Spinelli S, Sturla L, Guse A, De Flora A, Zocchi E, Heeren J, Bruzzone S
NUTRIENTS. 2021;13(11):.
CD38 downregulation modulates NAD+ and NADP(H) levels in thermogenic adipose tissues
Benzi A, Sturla L, Heine M, Fischer A, Spinelli S, Magnone M, Sociali G, Parodi A, Fenoglio D, Emionite L, Koch-Nolte F, Mittrücker H, Guse A, De Flora A, Zocchi E, Heeren J, Bruzzone S
BBA-MOL CELL BIOL L. 2021;1866(1):158819.
Nanoparticle-mediated targeting of autoantigen peptide to cross-presenting liver sinusoidal endothelial cells protects from CD8 T-cell-driven autoimmune cholangitis
Carambia A, Gottwick C, Schwinge D, Stein S, Digigow R, Şeleci M, Mungalpara D, Heine M, Schuran F, Corban C, Lohse A, Schramm C, Heeren J, Herkel J
IMMUNOLOGY. 2021;162(4):452-463.
Role of bile acids in inflammatory liver diseases
Evangelakos I, Heeren J, Verkade E, Kuipers F
SEMIN IMMUNOPATHOL. 2021;43(4):577-590.
Oxysterol 7-α Hydroxylase (CYP7B1) Attenuates Metabolic-Associated Fatty Liver Disease in Mice at Thermoneutrality
Evangelakos I, Schwinge D, Worthmann A, John C, Roeder N, Pertzborn P, Behrens J, Schramm C, Scheja L, Heeren J
CELLS-BASEL. 2021;10(10):2656.
Lysosomal lipoprotein processing in endothelial cells stimulates adipose tissue thermogenic adaptation
Fischer A, Jaeckstein M, Gottschling K, Heine M, Sass F, Mangels N, Schlein C, Worthmann A, Bruns O, Yuan Y, Zhu H, Chen O, Ittrich H, Nilsson S, Stefanicka P, Ukropec J, Balaz M, Dong H, Sun W, Reimer R, Scheja L, Heeren J
CELL METAB. 2021;33(3):547-564.e7.
Dual NADPH oxidases DUOX1 and DUOX2 synthesize NAADP and are necessary for Ca2+ signaling during T cell activation
Gu F, Krüger A, Roggenkamp H, Alpers R, Lodygin D, Jaquet V, Möckl F, Hernandez C L, Winterberg K, Bauche A, Rosche A, Grasberger H, Kao J, Schetelig D, Werner R, Schröder K, Carty M, Bowie A, Huber S, Meier C, Mittrücker H, Heeren J, Krause K, Flügel A, Diercks B, Guse A
SCI SIGNAL. 2021;14(709):.
Isthmin 1 - a novel insulin-like adipokine
Heeren J, Scheja L
NAT REV ENDOCRINOL. 2021;17(12):709-710.
Metabolic-associated fatty liver disease and lipoprotein metabolism
Heeren J, Scheja L
MOL METAB. 2021;50:101238.
Comment on “Mice Lacking the Purinergic Receptor P2X5 Exhibit Defective Inflammasome Activation and Early Susceptibility to Listeria monocytogenes”
Rissiek B, Heeren J, Koch-Nolte F, Mittrücker H, Magnus T
J IMMUNOL. 2021;206(4):.
TFEB-deficiency attenuates mitochondrial degradation upon brown adipose tissue whitening at thermoneutrality
Sass F, Schlein C, Jaeckstein M, Pertzborn P, Schweizer M, Schinke T, Ballabio A, Scheja L, Heeren J, Fischer A
MOL METAB. 2021;47:101173.
Endothelial Lipase Is Involved in Cold-Induced High-Density Lipoprotein Turnover and Reverse Cholesterol Transport in Mice
Schaltenberg N, John C, Heine M, Haumann F, Rinninger F, Scheja L, Heeren J, Worthmann A
FRONT CARDIOVASC MED. 2021;8:628235.
Endogenous Fatty Acid Synthesis Drives Brown Adipose Tissue Involution
Schlein C, Fischer A, Sass F, Worthmann A, Tödter K, Jaeckstein M, Behrens J, Lynes M, Kiebish M, Narain N, Bussberg V, Jespersen N, Nielsen S, Scheele C, Schweizer M, Braren I, Bartelt A, Tseng Y, Heeren J, Scheja L
CELL REP. 2021;34(2):108624.
Aryl Hydrocarbon Receptor Activity in Hepatocytes Sensitizes to Hyperacute Acetaminophen-Induced Hepatotoxicity in Mice
Schuran F, Lommetz C, Steudter A, Ghallab A, Wieschendorf B, Schwinge D, Zuehlke S, Reinders J, Heeren J, Lohse A, Schramm C, Herkel J, Carambia A
CELL MOL GASTROENTER. 2021;11(2):371-388.
Apolipoprotein E4 disrupts the neuroprotective action of sortilin in neuronal lipid metabolism and endocannabinoid signaling
Asaro A, Carlo-Spiewok A, Malik A, Rothe M, Schipke C, Peters O, Heeren J, Willnow T
ALZHEIMERS DEMENT. 2020;16(9):1248-1258.
Brown adipose tissue lipoprotein and glucose disposal is not determined by thermogenesis in uncoupling protein 1-deficient mice
Fischer A, Behrens J, Sass F, Schlein C, Heine M, Pertzborn P, Scheja L, Heeren J
J LIPID RES. 2020;61(11):1377-1389.
Thermoneutrality-Induced Macrophage Accumulation in Brown Adipose Tissue Does Not Impair the Tissue's Competence for Cold-Induced Thermogenic Recruitment
Fischer A, de Jong J, Sass F, Schlein C, Heeren J, Petrovic N
FRONT ENDOCRINOL. 2020;11:568682.
Therapeutic Targeting of Myeloperoxidase Attenuates NASH in Mice
Koop A, Thiele N, Steins D, Michaëlsson E, Wehmeyer M, Scheja L, Steglich B, Huber S, Schulze zur Wiesch J, Lohse A, Heeren J, Kluwe J
HEPATOL COMMUN. 2020;4(10):1441-1458.
Alterations of the bile microbiome in primary sclerosing cholangitis
Liwinski T, Zenouzi R, John C, Ehlken H, Rühlemann M, Bang C, Groth S, Lieb W, Kantowski M, Andersen N, Schachschal G, Karlsen T, Hov J, Rösch T, Lohse A, Heeren J, Franke A, Schramm C
GUT. 2020;69(4):665-672.
Annexin A6 modulates TBC1D15/Rab7/StARD3 axis to control endosomal cholesterol export in NPC1 cells
Meneses-Salas E, García-Melero A, Kanerva K, Blanco-Muñoz P, Morales-Paytuvi F, Bonjoch J, Casas J, Egert A, Beevi S, Jose J, Llorente-Cortés V, Rye K, Heeren J, Lu A, Pol A, Tebar F, Ikonen E, Grewal T, Enrich C, Rentero C
CELL MOL LIFE SCI. 2020;77(14):2839-2857.
Development of the Metabolic Syndrome: Study Design and Baseline Data of the Lufthansa Prevention Study (LUPS), A Prospective Observational Cohort Survey.
Müller-Wieland D, Altenburg C, Becher H, Burchard J, Frisch A, Gebhard J, Haas J, Harth V, Heeren J, Hengelbrock J, von Karais M, Knebel B, Kotzka J, Löwe B, Marx N, Pinnschmidt H, Preisser A, Rose M, Sawitzky-Rose B, Scheja L, Terschüren C, Töller M, Vettorazzi E, Wegscheider K
EXP CLIN ENDOCR DIAB. 2020;128(12):777-787.
Inulin Supplementation Disturbs Hepatic Cholesterol and Bile Acid Metabolism Independent from Housing Temperature
Pauly M, Rohde J, John C, Evangelakos I, Koop A, Pertzborn P, Tödter K, Scheja L, Heeren J, Worthmann A
NUTRIENTS. 2020;12(10):.
A MAFG-lncRNA axis links systemic nutrient abundance to hepatic glucose metabolism
Pradas-Juni M, Hansmeier N, Link J, Schmidt E, Larsen B, Klemm P, Meola N, Topel H, Loureiro R, Dhaouadi I, Kiefer C, Schwarzer R, Khani S, Oliverio M, Awazawa M, Frommolt P, Heeren J, Scheja L, Heine M, Dieterich C, Büning H, Yang L, Cao H, Jesus D, Kulkarni R, Zevnik B, Tröder S, Knippschild U, Edwards P, Lee R, Yamamoto M, Ulitsky I, Fernandez-Rebollo E, Vallim T, Kornfeld J
NAT COMMUN. 2020;11(1):644.
The P2X7 ion channel is dispensable for energy and metabolic homeostasis of white and brown adipose tissues
Tian T, Heine M, Evangelakos I, Jaeckstein M, Schaltenberg N, Stähler T, Koch-Nolte F, Kumari M, Heeren J
PURINERG SIGNAL. 2020;16(4):529-542.
Abscisic acid stimulates the release of insulin and of GLP-1 in the rat perfused pancreas and intestine
Booz V, Christiansen C, Kuhre R, Saltiel M, Sociali G, Schaltenberg N, Fischer A, Heeren J, Zocchi E, Holst J, Bruzzone S
DIABETES-METAB RES. 2019;35(2):e3102.
PID1 regulates insulin-dependent glucose uptake by controlling intracellular sorting of GLUT4-storage vesicles
Fischer A, Albers K, Schlein C, Sass F, Krott L, Schmale H, Gordts P, Scheja L, Heeren J
BBA-MOL BASIS DIS. 2019;1865(6):1592-1603.
Intact innervation is essential for diet-induced recruitment of brown adipose tissue
Fischer A, Schlein C, Cannon B, Heeren J, Nedergaard J
AM J PHYSIOL-ENDOC M. 2019;316(3):E487-E503.
Adenine nucleotides as paracrine mediators and intracellular second messengers in immunity and inflammation
Fliegert R, Heeren J, Koch-Nolte F, Nikolaev V, Lohr C, Meier C, Guse A
BIOCHEM SOC T. 2019;47(1):329-337.
Liver infiltrating T cells regulate bile acid metabolism in experimental cholangitis
Glaser F, John C, Engel B, Höh B, Weidemann S, Dieckhoff J, Stein S, Becker N, Casar C, Amrei Schuran F, Wieschendorf B, Preti M, Jessen F, Franke A, Carambia A, Lohse A, Ittrich H, Herkel J, Heeren J, Schramm C, Schwinge D
J HEPATOL. 2019;71(4):783-792.
Lysosomal integral membrane protein-2 (LIMP-2/SCARB2) is involved in lysosomal cholesterol export
Heybrock S, Kanerva K, Meng Y, Ing C, Liang A, Xiong Z, Weng X, Ah Kim Y, Collins R, Trimble W, Pomès R, Privé G, Annaert W, Schwake M, Heeren J, Lüllmann-Rauch R, Grinstein S, Ikonen E, Saftig P, Neculai D
NAT COMMUN. 2019;10(1):3521.
Thyroid-Hormone-Induced Browning of White Adipose Tissue Does Not Contribute to Thermogenesis and Glucose Consumption
Johann K, Cremer A, Fischer A, Heine M, Pensado E, Resch J, Nock S, Virtue S, Harder L, Oelkrug R, Astiz M, Brabant G, Warner A, Vidal-Puig A, Oster H, Boelen A, López M, Heeren J, Dalley J, Backes H, Mittag J
CELL REP. 2019;27(11):3385-3400.e3.
Scanning transmission X-ray microscopy with efficient X-ray fluorescence detection (STXM-XRF) for biomedical applications in the soft and tender energy range
Lühl L, Andrianov K, Dierks H, Haidl A, Dehlinger A, Heine M, Heeren J, Nisius T, Wilhein T, Kanngießer B
J SYNCHROTRON RADIAT. 2019;26(Pt 2):430-438.
The endocrine function of adipose tissues in health and cardiometabolic disease
Scheja L, Heeren J
NAT REV ENDOCRINOL. 2019;15(9):507-524.
Effects of Pharmacological Thermogenic Adipocyte Activation on Metabolism and Atherosclerotic Plaque Regression
Worthmann A, Schlein C, Berbée J, Rensen P, Heeren J, Bartelt A
NUTRIENTS. 2019;11(2):.
Lrp1 in osteoblasts controls osteoclast activity and protects against osteoporosis by limiting PDGF-RANKL signaling
Bartelt A, Behler-Janbeck F, Beil F, Koehne T, Müller B, Schmidt T, Heine M, Ochs L, Yilmaz T, Dietrich M, Tuckermann J, Amling M, Herz J, Schinke T, Heeren J, Niemeier A
BONE RES. 2018;6:4.
Altered hepatic glucose homeostasis in AnxA6-KO mice fed a high-fat diet
Cairns R, Fischer A, Blanco-Munoz P, Alvarez-Guaita A, Meneses-Salas E, Egert A, Buechler C, Hoy A, Heeren J, Enrich C, Rentero C, Grewal T
PLOS ONE. 2018;13(8):e0201310.
The Apolipoprotein M/S1P Axis Controls Triglyceride Metabolism and Brown Fat Activity
Christoffersen C, Federspiel C, Borup A, Christensen P, Madsen A, Heine M, Nielsen C, Kjaer A, Holst B, Heeren J, Nielsen L
CELL REP. 2018;22(1):175-188.
The adaptor protein PID1 regulates receptor-dependent endocytosis of postprandial triglyceride-rich lipoproteins
Fischer A, Albers K, Krott L, Hoffzimmer B, Heine M, Schmale H, Scheja L, Gordts P, Heeren J
MOL METAB. 2018;16:88-99.
Brown adipose tissue and lipid metabolism
Heeren J, Scheja L
CURR OPIN LIPIDOL. 2018;29(3):180-185.
Lipolysis Triggers a Systemic Insulin Response Essential for Efficient Energy Replenishment of Activated Brown Adipose Tissue in Mice
Heine M, Fischer A, Schlein C, Jung C, Straub L, Gottschling K, Mangels N, Yuan Y, Nilsson S, Liebscher G, Chen O, Schreiber R, Zechner R, Scheja L, Heeren J
CELL METAB. 2018;28(4):644-655.e4.
Regulation of immunometabolism in adipose tissue
Kumari M, Heeren J, Scheja L
SEMIN IMMUNOPATHOL. 2018;40(2):189-202.
FoxO transcription factors are required for hepatic HDL-cholesterol clearance
Lee S, Heine M, Schlein C, Ramakrishnan R, Liu J, Belnavis G, Haimi I, Fischer A, Ginsberg H, Heeren J, Rinninger F, Haeusler R
J CLIN INVEST. 2018;128(4):1615-1626.
Naturally Occurring Variants in LRP1 (Low-Density Lipoprotein Receptor-Related Protein 1) Affect HDL (High-Density Lipoprotein) Metabolism Through ABCA1 (ATP-Binding Cassette A1) and SR-B1 (Scavenger Receptor Class B Type 1) in Humans
Oldoni F, van Capelleveen J, Dalila N, Wolters J, Heeren J, Sinke R, Hui D, Dallinga-Thie G, Frikke-Schmidt R, Hovingh K, van de Sluis B, Tybjærg-Hansen A, Kuivenhoven J
ARTERIOSCL THROM VAS. 2018;38(7):1440-1453.
Introduction to the special issue on dietary control of immunometabolism
Scheja L, Heeren J
SEMIN IMMUNOPATHOL. 2018;40(2):141-144.
LincRNA H19 protects from dietary obesity by constraining expression of monoallelic genes in brown fat
Schmidt E, Dhaouadi I, Gaziano I, Oliverio M, Klemm P, Awazawa M, Mitterer G, Fernandez-Rebollo E, Pradas-Juni M, Wagner W, Hammerschmidt P, Loureiro R, Kiefer C, Hansmeier N, Khani S, Bergami M, Heine M, Ntini E, Frommolt P, Zentis P, Ørom U, Heeren J, Blüher M, Bilban M, Kornfeld J
NAT COMMUN. 2018;9(1):3622.
Dietary protein restriction reduces circulating VLDL triglyceride levels via CREBH-APOA5-dependent and -independent mechanisms
Treviño-Villarreal J, Reynolds J, Bartelt A, Langston P, MacArthur M, Arduini A, Tosti V, Veronese N, Bertozzi B, Brace L, Mejia P, Trocha K, Kajitani G, Longchamp A, Harputlugil E, Gathungu R, Bird S, Bullock A, Figenshau R, Andriole G, Thompson A, Heeren J, Ozaki C, Kristal B, Fontana L, Mitchell J
JCI INSIGHT. 2018;3(21):.
Assessment of Uptake and Biodistribution of Radiolabeled Cholesterol in Mice Using Gavaged Recombinant Triglyceride-rich Lipoprotein Particles (rTRL)
Worthmann A, John C, Heeren J
BIO-PROTOCOL. 2018;8(13):e2916.
AMPK Prevents Palmitic Acid-Induced Apoptosis and Lipid Accumulation in Cardiomyocytes
Adrian L, Lenski M, Tödter K, Heeren J, Böhm M, Laufs U
LIPIDS. 2017;52(9):737-750.
Differential effects of Calca-derived peptides in male mice with diet-induced obesity
Bartelt A, Jeschke A, Müller B, Gaziano I, Morales M, Yorgan T, Heckt T, Heine M, Gagel R, Emeson R, Amling M, Niemeier A, Heeren J, Schinke T, Keller J
PLOS ONE. 2017;12(6):e0180547.
Thermogenic adipocytes promote HDL turnover and reverse cholesterol transport
Bartelt A, John C, Schaltenberg N, Berbée J, Worthmann A, Cherradi M, Schlein C, Piepenburg J, Boon M, Rinninger F, Heine M, Toedter K, Niemeier A, Nilsson S, Fischer M, Wijers S, van Marken Lichtenbelt W, Scheja L, Rensen P, Heeren J
NAT COMMUN. 2017;8:Art. 15010.
Quantification of Bone Fatty Acid Metabolism and Its Regulation by Adipocyte Lipoprotein Lipase
Bartelt A, Koehne T, Tödter K, Reimer R, Müller B, Behler-Janbeck F, Heeren J, Scheja L, Niemeier A
INT J MOL SCI. 2017;18(6):1264.
Next-Generation optical imaging with short-wave infrared quantum dots
Bruns O, Bischof T, Harris D, Franke D, Shi Y, Riedemann L, Bartelt A, Jaworski F, Carr J, Rowlands C, Wilson M, Chen O, Wei H, Hwang G, Montana D, Coropceanu I, Achorn O, Kloepper J, Heeren J, So P, Fukumura D, Jensen K, Jain R, Bawendi M
NAT BIOMED ENG. 2017;1(4):UNSP 0056.
Metabolic Circuit Involving Free Fatty Acids, microRNA 122, and Triglyceride Synthesis in Liver and Muscle Tissues
Chai C, Rivkin M, Berkovits L, Simerzin A, Zorde-Khvalevsky E, Rosenberg N, Klein S, Yaish D, Durst R, Shpitzen S, Udi S, Tam J, Heeren J, Worthmann A, Schramm C, Kluwe J, Ravid R, Hornstein E, Giladi H, Galun E
GASTROENTEROLOGY. 2017;153(5):1404-1415.
Cold-Induced Brown Adipose Tissue Activity Alters Plasma Fatty Acids and Improves Glucose Metabolism in Men
Iwen K, Backhaus J, Cassens M, Waltl M, Hedesan O, Merkel M, Heeren J, Sina C, Rademacher L, Windjäger A, Haug A, Kiefer F, Lehnert H, Schmid S
J CLIN ENDOCR METAB. 2017;102(11):4226-4234.
Quantitative and qualitative estimation of atherosclerotic plaque burden in vivo at 7T MRI using Gadospin F in comparison to en face preparation evaluated in ApoE KO mice
Jung C, Christiansen S, Kaul M, Koziolek E, Reimer R, Heeren J, Adam G, Heine M, Ittrich H
PLOS ONE. 2017;12(8):e0180407.
Disruption of the vacuolar-type H-ATPase complex in liver causes MTORC1-independent accumulation of autophagic vacuoles and lysosomes
Kissing S, Rudnik S, Damme M, Lüllmann-Rauch R, Ichihara A, Kornak U, Eskelinen E, Jabs S, Heeren J, De Brabander J, Haas A, Saftig P
AUTOPHAGY. 2017;13(4):670-685.
The TREM2-APOE Pathway Drives the Transcriptional Phenotype of Dysfunctional Microglia in Neurodegenerative Diseases
Krasemann S, Madore C, Cialic R, Baufeld C, Calcagno N, El Fatimy R, Beckers L, O'Loughlin E, Xu Y, Fanek Z, Greco D, Smith S, Tweet G, Humulock Z, Zrzavy T, Conde-Sanroman P, Gacias M, Weng Z, Chen H, Tjon E, Mazaheri F, Hartmann K, Madi A, Ulrich J, Glatzel M, Worthmann A, Heeren J, Budnik B, Lemere C, Ikezu T, Heppner F, Litvak V, Holtzman D, Lassmann H, Weiner H, Ochando J, Haass C, Butovsky O
IMMUNITY. 2017;47(3):566-581.e9.
The TMAO-Producing Enzyme Flavin-Containing Monooxygenase 3 Regulates Obesity and the Beiging of White Adipose Tissue
Schugar R, Shih D, Warrier M, Helsley R, Burrows A, Ferguson D, Brown A, Gromovsky A, Heine M, Chatterjee A, Li L, Li X, Wang Z, Willard B, Meng Y, Kim H, Che N, Pan C, Lee R, Crooke R, Graham M, Morton R, Langefeld C, Das S, Rudel L, Zein N, McCullough A, Dasarathy S, Tang W, Erokwu B, Flask C, Laakso M, Civelek M, Naga Prasad S, Heeren J, Lusis A, Hazen S, Brown J
CELL REP. 2017;19(12):2451-2461.
The TMAO-Producing Enzyme Flavin-Containing Monooxygenase 3 Regulates Obesity and the Beiging of White Adipose Tissue (vol 19, pg 2451, 2017)
Schugar R, Shih D, Warrier M, Helsley R, Burrows A, Ferguson D, Brown A, Gromovsky A, Heine M, Chatterjee A, Li L, Li X, Wang Z, Willard B, Meng Y, Kim H, Che N, Pan C, Lee R, Crooke R, Graham M, Morton R, Langefeld C, Das S, Rudel L, Zein N, McCullough A, Dasarathy S, Tang W, Erokwu B, Flask C, Laakso M, Civelek M, Naga Prasad S, Heeren J, Lusis A, Hazen S, Brown J
CELL REP. 2017;20(1):279.
Cold-induced conversion of cholesterol to bile acids in mice shapes the gut microbiome and promotes adaptive thermogenesis
Worthmann A, John C, Rühlemann M, Baguhl M, Heinsen F, Schaltenberg N, Heine M, Schlein C, Evangelakos I, Mineo C, Fischer M, Dandri M, Kremoser C, Scheja L, Franke A, Shaul P, Heeren J
NAT MED. 2017;23(7):839-849.
Exosomal microRNA miR-92a concentration in serum reflects human brown fat activity
Chen Y, Buyel J, Hanssen M, Siegel F, Pan R, Naumann J, Schell M, van der Lans A, Schlein C, Froehlich H, Heeren J, Virtanen K, van Marken Lichtenbelt W, Pfeifer A
NAT COMMUN. 2016;7:11420.
Novel Mouse Models of Methylmalonic Aciduria Recapitulate Phenotypic Traits with a Genetic Dosage Effect
Forny P, Schumann A, Mustedanagic M, Mathis D, Wulf M, Naegele N, Langhans C, Zhakupova A, Heeren J, Scheja L, Fingerhut R, Peters H, Hornemann T, Thony B, Koelker S, Burda P, Froese D, Devuyst O, Baumgartner M
J BIOL CHEM. 2016;291(39):20563-73.
Investigation of the anti-obesity effect of Pueraria montana var. lobata
Houriet J, Buhlmann E, Rudigier C, Kiehlmann E, Radtke J, Heeren J, Friedemann T, Schröder S, Wolfrum C, Wolfender J
PLANTA MED. 2016;81(S 01):S1-S381.
Quantitative Activity Measurements of Brown Adipose Tissue at 7 T Magnetic Resonance Imaging After Application of Triglyceride-Rich Lipoprotein 59Fe-Superparamagnetic Iron Oxide Nanoparticle: Intravenous Versus Intraperitoneal Approach
Jung C, Heine M, Freund B, Reimer R, Koziolek E, Kaul M, Kording F, Schumacher U, Weller H, Nielsen P, Adam G, Heeren J, Ittrich H
INVEST RADIOL. 2016;51(3):194-202.
Attenuated viral hepatitis in Trem1-/- mice is associated with reduced inflammatory activity of neutrophils
Kozik J, Trautmann T, Carambia A, Preti M, Lütgehetmann M, Krech T, Wiegard C, Heeren J, Herkel J
SCI REP-UK. 2016;6:28556.
Endocannabinoid regulation in white and brown adipose tissue following thermogenic activation
Krott L, Piscitelli F, Heine M, Borrino S, Scheja L, Silvestri C, Heeren J, Di Marzo V
J LIPID RES. 2016;57(3):464-73.
Dicer1-miR-328-Bace1 signalling controls brown adipose tissue differentiation and function
Oliverio M, Schmidt E, Mauer J, Baitzel C, Hansmeier N, Khani S, Konieczka S, Pradas-Juni M, Brodesser S, Van T, Bartsch D, Brönneke H, Heine M, Hilpert H, Tarcitano E, Garinis G, Frommolt P, Heeren J, Mori M, Brüning J, Kornfeld J
NAT CELL BIOL. 2016;18(3):328-36.
Metabolic interplay between white, beige, brown adipocytes and the liver
Scheja L, Heeren J
J HEPATOL. 2016;64(5):1176-86.
Insulin Regulates Hepatic Triglyceride Secretion and Lipid Content via Signaling in the Brain
Scherer T, Lindtner C, O'Hare J, Hackl M, Zielinski E, Freudenthaler A, Baumgartner-Parzer S, Tödter K, Heeren J, Krššák M, Scheja L, Fürnsinn C, Buettner C
DIABETES. 2016;65(6):1511-20.
Implications of thermogenic adipose tissues for metabolic health
Schlein C, Heeren J
BEST PRACT RES CL EN. 2016;30(4):487-496.
FGF21 Lowers Plasma Triglycerides by Accelerating Lipoprotein Catabolism in White and Brown Adipose Tissues
Schlein C, Talukdar S, Heine M, Fischer A, Krott L, Nilsson S, Brenner M, Heeren J, Scheja L
CELL METAB. 2016;23(3):441-53.
Mitochondrial gene polymorphisms alter hepatic cellular energy metabolism and aggravate diet-induced non-alcoholic steatohepatitis
Schröder T, Kucharczyk D, Bär F, Pagel R, Derer S, Jendrek S, Sünderhauf A, Brethack A, Hirose M, Möller S, Künstner A, Bischof J, Weyers I, Heeren J, Koczan D, Schmid S, Divanovic S, Giles D, Adamski J, Fellermann K, Lehnert H, Köhl J, Ibrahim S, Sina C
CELL METAB. 2016;5(4):283-95.
Utilizing immunoaffinity chromatography (IAC) cross-reactivity in GC-MS/MS exemplified at the measurement of prostaglandin E1 in human plasma using prostaglandin E2-specific IAC columns
Tsikas D, Suchy M, Tödter K, Heeren J, Scheja L
J CHROMATOGR B. 2016;1021:101-7.
The distribution and degradation of radiolabeled superparamagnetic iron oxide nanoparticles and quantum dots in mice
Bargheer D, Giemsa A, Freund B, Heine M, Waurisch C, Stachowski G, Hickey S, Eychmüller A, Heeren J, Nielsen P
BEILSTEIN J NANOTECH. 2015;6:111-23.
The fate of a designed protein corona on nanoparticles in vitro and in vivo
Bargheer D, Nielsen J, Gébel G, Heine M, Salmen S, Stauber R, Weller H, Heeren J, Nielsen P
BEILSTEIN J NANOTECH. 2015;6:36-46.
Caloric restriction and intermittent fasting alter hepatic lipid droplet proteome and diacylglycerol species and prevent diabetes in NZO mice
Baumeier C, Kaiser D, Heeren J, Scheja L, John C, Weise C, Eravci M, Lagerpusch M, Schulze G, Joost H, Schwenk R, Schürmann A
Biochim Biophys Acta. 2015;1851(5):566-76.
Brown fat activation reduces hypercholesterolaemia and protects from atherosclerosis development
Berbée J, Boon M, Khedoe P, Bartelt A, Schlein C, Worthmann A, Kooijman S, Hoeke G, Mol I, John C, Jung C, Vazirpanah N, Brouwers L, Gordts P, Esko J, Hiemstra P, Havekes L, Scheja L, Heeren J, Rensen P
NAT COMMUN. 2015;6:6356.
Nanoparticle-based autoantigen delivery to Treg-inducing liver sinusoidal endothelial cells enables control of autoimmunity in mice
Carambia A, Freund B, Schwinge D, Bruns O, Salmen S, Ittrich H, Reimer R, Heine M, Huber S, Waurisch C, Eychmüller A, Wraith D, Korn T, Nielsen P, Weller H, Schramm C, Lüth S, Lohse A, Heeren J, Herkel J
J HEPATOL. 2015;62(6):1349-1356.
ANGPTL4 mediates shuttling of lipid fuel to brown adipose tissue during sustained cold exposure
Dijk W, Heine M, Vergnes L, Boon M, Schaart G, Hesselink M, Reue K, van Marken Lichtenbelt W, Olivecrona G, Rensen P, Heeren J, Kersten S
ELIFE. 2015;4:.
Stimulation of soluble guanylyl cyclase protects against obesity by recruiting brown adipose tissue
Hoffmann L, Etzrodt J, Willkomm L, Sanyal A, Scheja L, Fischer A, Stasch J, Bloch W, Friebe A, Heeren J, Pfeifer A
NAT COMMUN. 2015;6:Art. 7235.
Site-1 protease-activated formation of lysosomal targeting motifs is independent of the lipogenic transcription control
Klünder S, Heeren J, Markmann S, Santer R, Braulke T, Pohl S
J LIPID RES. 2015;56(8):1625-32.
Apolipoprotein E promotes lipid accumulation and differentiation in human adipocytes
Lasrich D, Bartelt A, Grewal T, Heeren J
EXP CELL RES. 2015;337(1):94-102.
Diabetes prevalence in NZO females depends on estrogen action on liver fat content
Lubura M, Hesse D, Krämer M, Hallahan N, Schupp M, Loeffelholz C, Kriebel J, Rudovich N, Pfeiffer A, John C, Scheja L, Heeren J, Koliaki C, Roden M, Schürmann A
AM J PHYSIOL-ENDOC M. 2015;309(12):E968-E980.
Lrp1/LDL receptor play critical roles in mannose 6-phosphate-independent lysosomal enzyme targeting
Markmann S, Thelen M, Cornils K, Schweizer M, Brocke-Ahmadinejad N, Willnow T, Heeren J, Gieselmann V, Braulke T, Kollmann K
TRAFFIC. 2015.
Genetic Dissection of Tissue-Specific Apolipoprotein E Function for Hypercholesterolemia and Diet-Induced Obesity
Wagner T, Bartelt A, Schlein C, Heeren J
PLOS ONE. 2015;10(12):.
Homozygosity for a partial deletion of apoprotein A-V signal peptide results in intracellular missorting of the protein and chylomicronemia in a breast-fed infant
Albers K, Schlein C, Wenner K, Lohse P, Bartelt A, Heeren J, Santer R, Merkel M
ATHEROSCLEROSIS. 2014;233(1):97-103.
Hepatic lipase is expressed by osteoblasts and modulates bone remodeling in obesity
Bartelt A, Beil T, Müller B, Koehne T, Yorgan T, Heine M, Yilmaz T, Ruether W, Heeren J, Schinke T, Niemeier A
BONE. 2014;62:90-98.
Adipose tissue browning and metabolic health
Bartelt A, Heeren J
NAT REV ENDOCRINOL. 2014;10(1):24-36.
TGF-β-dependent induction of CD4⁺CD25⁺Foxp3⁺ Tregs by liver sinusoidal endothelial cells
Carambia A, Freund B, Schwinge D, Heine M, Laschtowitz A, Huber S, Wraith D, Korn T, Schramm C, Lohse A, Heeren J, Herkel J
J HEPATOL. 2014;61(3):594-9.
Dichloroacetate prevents restenosis in preclinical animal models of vessel injury
Deuse T, Hua X, Wang D, Maegdefessel L, Heeren J, Scheja L, Bolaños J, Rakovic A, Spin J, Stubbendorff M, Ikeno F, Länger F, Zeller T, Schulte-Uentrop L, Stoehr A, Itagaki R, Haddad F, Eschenhagen T, Blankenberg S, Kiefmann R, Reichenspurner H, Velden J, Klein C, Yeung A, Robbins R, Tsao P, Schrepfer S
NATURE. 2014;509(7502):641-644.
Selectins mediate small cell lung cancer systemic metastasis
Heidemann F, Schildt A, Schmid K, Bruns O, Riecken K, Jung C, Ittrich H, Wicklein D, Reimer R, Fehse B, Heeren J, Lüers G, Schumacher U, Heine M
PLOS ONE. 2014;9(4):e92327.
The cell-type specific uptake of polymer-coated or micelle-embedded QDs and SPIOs does not provoke an acute pro-inflammatory response in the liver
Heine M, Bartelt A, Bruns O, Bargheer D, Giemsa A, Freund B, Scheja L, Waurisch C, Eychmüller A, Reimer R, Weller H, Nielsen P, Heeren J
BEILSTEIN J NANOTECH. 2014;5:1432-1440.
A liquid chromatography-tandem mass spectrometry-based method for the simultaneous determination of hydroxy sterols and bile acids
John C, Werner P, Worthmann A, Wegner K, Tödter K, Scheja L, Rohn S, Heeren J, Fischer M
J CHROMATOGR A. 2014;1371:184-195.
Intraperitoneal Injection Improves the Uptake of Nanoparticle-Labeled High-Density Lipoprotein to Atherosclerotic Plaques Compared With Intravenous Injection: A Multimodal Imaging Study in ApoE Knockout Mice
Jung C, Kaul M, Bruns O, Dučić T, Freund B, Heine M, Reimer R, Meents A, Salmen S, Weller H, Nielsen P, Adam G, Heeren J, Ittrich H
CIRC-CARDIOVASC IMAG. 2014;7(2):303-11.
Binding of hepatitis B virus to its cellular receptor alters the expression profile of genes of bile acid metabolism
Oehler N, Volz T, Bhadra O, Kah J, Allweiss L, Giersch K, Bierwolf J, Riecken K, Pollok J, Lohse A, Fehse B, Petersen J, Urban S, Lütgehetmann M, Heeren J, Dandri M
HEPATOLOGY. 2014.
Cholesterol Regulates Syntaxin 6 Trafficking at trans-Golgi Network Endosomal Boundaries
Reverter M, Rentero C, Garcia-Melero A, Hoque M, Vilà de Muga S, Alvarez-Guaita A, Conway J, Wood P, Cairns R, Lykopoulou L, Grinberg D, Vilageliu L, Bosch M, Heeren J, Blasi J, Timpson P, Pol A, Tebar F, Murray R, Grewal T, Enrich C
CELL REP. 2014;7(3):883-897.
High density lipoprotein metabolism in low density lipoprotein receptor-deficient mice
Rinninger F, Heine M, Singaraja R, Hayden M, Brundert M, Ramakrishnan R, Heeren J
J LIPID RES. 2014;55(9):1914-1924.
Synthesis of radioactively labelled CdSe/CdS/ZnS quantum dots for in vivo experiments
Stachowski G, Bauer C, Waurisch C, Bargheer D, Nielsen P, Heeren J, Hickey S, Eychmüller A
BEILSTEIN J NANOTECH. 2014;5:2383-2387.
Effects of adipocyte lipoprotein lipase on de novo lipogenesis and white adipose tissue browning
Bartelt A, John C, Cherradi M, Niemeier A, Tödter K, Heeren J, Scheja L
BBA-MOL CELL BIOL L. 2013;1831(5):934-42.
The pro-neurotrophin receptor sortilin is a major neuronal apolipoprotein E receptor for catabolism of amyloid-β peptide in the brain
Carlo A, Gustafsen C, Mastrobuoni G, Nielsen M, Burgert T, Hartl D, Rohe M, Nykjaer A, Herz J, Heeren J, Kempa S, Petersen C, Willnow T
J NEUROSCI. 2013;33(1):358-70.
Pharmacological characterization of 1-nitrosocyclohexyl acetate, a long-acting nitroxyl donor that shows vasorelaxant and antiaggregatory effects
Donzelli S, Fischer G, King B, Niemann C, DuMond J, Heeren J, Wieboldt H, Baldus S, Gerloff C, Eschenhagen T, Carrier L, Böger R, Espey M
J PHARMACOL EXP THER. 2013;344(2):339-47.
De novo lipogenesis in human fat and liver is linked to ChREBP-β and metabolic health
Eissing L, Scherer T, Tödter K, Knippschild U, Greve J, Buurman W, Pinnschmidt H, Rensen S, Wolf A, Bartelt A, Heeren J, Buettner C, Scheja L
NAT COMMUN. 2013;4:1528.
Novel aspects of brown adipose tissue biology
Heeren J, Münzberg H
ENDOCRIN METAB CLIN. 2013;42(1):89-107.
TNFα-mediated liver destruction by Kupffer cells and Ly6Chi monocytes during Entamoeba histolytica infection
Helk E, Bernin H, Ernst T, Ittrich H, Jacobs T, Heeren J, Tacke F, Tannich E, Lotter H
PLOS PATHOG. 2013;9(1):e1003096.
Obesity-induced overexpression of miR-802 impairs glucose metabolism through silencing of Hnf1b
Kornfeld J, Baitzel C, Könner A, Nicholls H, Vogt M, Herrmanns K, Scheja L, Haumaitre C, Wolf A, Knippschild U, Seibler J, Cereghini S, Heeren J, Stoffel M, Brüning J
NATURE. 2013;494(7435):111-5.
Inhibition of mitogen-activated protein kinase Erk1/2 promotes protein degradation of ATP binding cassette transporters A1 and G1 in CHO and HuH7 cells
Mulay V, Wood P, Manetsch M, Darabi M, Cairns R, Hoque M, Chan K, Reverter M, Alvarez-Guaita A, Rye K, Rentero C, Heeren J, Enrich C, Grewal T
PLOS ONE. 2013;8(4):e62667.
Increased expression of transthyretin in leptin-deficient ob/ob mice is not causative for their major phenotypic abnormalities.
Rendenbach C, Ganswindt S, Seitz S, Barvencik F, Hübner A, Baranowsky A, Streichert T, Niemeier A, Heeren J, Amling M, Bartelt A, Schinke T
J NEUROENDOCRINOL. 2013;25(1):14-22.
The holy grail of metabolic disease: brown adipose tissue.
Bartelt A, Heeren J
CURR OPIN LIPIDOL. 2012;23(3):190-195.
A new, powerful player in lipoprotein metabolism: brown adipose tissue.
Bartelt A, Merkel M, Heeren J
J MOL MED. 2012;90(8):887-893.
A simple and widely applicable method to 59Fe-radiolabel monodisperse superparamagnetic iron oxide nanoparticles for in vivo quantification studies.
Freund B, Tromsdorf U, Bruns O, Heine M, Giemsa A, Bartelt A, Salmen S, Raabe N, Heeren J, Ittrich H, Reimer R, Hohenberg H, Schumacher U, Weller H, Nielsen P
ACS NANO. 2012;6(8):7318-7325.
Impaired LDL receptor-related protein 1 translocation correlates with improved dyslipidemia and atherosclerosis in apoE-deficient mice.
Gordts P, Bartelt A, Nilsson S, Annaert W, Christoffersen C, Nielsen L, Heeren J, Roebroek A
PLOS ONE. 2012;7(6):38330.
Nanocrystals, a new tool to study lipoprotein metabolism and atherosclerosis.
Heeren J, Bruns O
CURR PHARM BIOTECHNO. 2012;13(2):365-372.
The GTPase ARFRP1 controls the lipidation of chylomicrons in the Golgi of the intestinal epithelium.
Jaschke A, Chung B, Hesse D, Kluge R, Zahn C, Moser M, Petzke K, Brigelius-Flohé R, Puchkov D, Koepsell H, Heeren J, Joost H, Schürmann A
HUM MOL GENET. 2012;21(14):3128-3142.
Low density lipoprotein receptor-related protein 1 dependent endosomal trapping and recycling of apolipoprotein E.
Laatsch A, Panteli M, Sornsakrin M, Hoffzimmer B, Grewal T, Heeren J
PLOS ONE. 2012;7(1):29385.
Mannose 6 dephosphorylation of lysosomal proteins mediated by acid phosphatases Acp2 and Acp5.
Makrypidi G, Damme M, Müller-Loennies S, Trusch M, Schmidt B, Schlüter H, Heeren J, Lübke T, Saftig P, Braulke T
MOL CELL BIOL. 2012;32(4):774-782.
The role of apolipoprotein E in bone metabolism.
Niemeier A, Schinke T, Heeren J, Amling M
BONE. 2012;50(2):518-524.
Triacylglycerol-rich lipoproteins protect lipoprotein lipase from inactivation by ANGPTL3 and ANGPTL4.
Nilsson S, Anderson F, Ericsson M, Larsson M, Makoveichuk E, Lookene A, Heeren J, Olivecrona G
Biochim Biophys Acta. 2012;1821(10):1370-1378.
The 5-phosphatase OCRL mediates retrograde transport of the mannose 6-phosphate receptor by regulating a Rac1-cofilin signalling module.
van Rahden V, Brand K, Najm J, Heeren J, Heeren J, Braulke T, Kutsche K, Kutsche K
HUM MOL GENET. 2012;21(23):5019-5038.
Brown adipose tissue activity controls triglyceride clearance.
Bartelt A, Bruns O, Reimer R, Hohenberg H, Ittrich H, Peldschus K, Kaul M, Tromsdorf U, Weller H, Waurisch C, Eychmüller A, Gordts P, Rinninger F, Brügelmann K, Freund B, Nielsen P, Merkel M, Heeren J
NAT MED. 2011;17(2):200-205.
Altered endocannabinoid signalling after a high-fat diet in Apoe(-/-) mice: relevance to adipose tissue inflammation, hepatic steatosis and insulin resistance.
Bartelt A, Orlando P, Mele C, Ligresti A, Tödter K, Scheja L, Heeren J, Di Marzo V
DIABETOLOGIA. 2011;54(11):2900-2910.
Scavenger receptor CD36 mediates uptake of high density lipoproteins in mice and by cultured cells.
Brundert M, Heeren J, Merkel M, Carambia A, Herkel J, Groitl P, Dobner T, Ramakrishnan R, Moore K, Rinninger F
J LIPID RES. 2011;52(4):745-758.
PML isoforms I and II participate in PML-dependent restriction of HSV-1 replication.
Cuchet D, Sykes A, Nicolas A, Orr A, Murray J, Sirma H, Heeren J, Bartelt A, Everett R
J CELL SCI. 2011;124(2):280-291.
[Energy, brown adipose tissue, obesity].
Merkel M, Heeren J
DEUT MED WOCHENSCHR. 2011;136(11):548-550.
Apolipoprotein A-V; a potent triglyceride reducer.
Nilsson S, Heeren J, Olivecrona G, Merkel M
ATHEROSCLEROSIS. 2011;219(1):15-21.
Short-term activation of liver X receptors inhibits osteoblasts but long-term activation does not have an impact on murine bone in vivo.
Prawitt J, Beil F, Marshall R, Bartelt A, Rüther W, Heeren J, Amling M, Staels B, Niemeier A
BONE. 2011;48(2):339-346.
Role for LAMP-2 in endosomal cholesterol transport.
Schneede A, Schmidt C, Hölttä-Vuori M, Heeren J, Willenborg M, Blanz J, Domanskyy M, Breiden B, Brodesser S, Landgrebe J, Sandhoff K, Ikonen E, Saftig P, Eskelinen E
J CELL MOL MED. 2011;15(2):280-295.
Ras/mitogen-activated protein kinase (MAPK) signaling modulates protein stability and cell surface expression of scavenger receptor SR-BI.
Wood P, Mulay V, Darabi M, Chan K, Heeren J, Pol A, Lambert G, Rye K, Enrich C, Grewal T
J BIOL CHEM. 2011;286(26):23077-23092.
Apolipoprotein E-dependent inverse regulation of vertebral bone and adipose tissue mass in C57Bl/6 mice: modulation by diet-induced obesity.
Bartelt A, Beil F, Schinke T, Röser K, Ruether W, Heeren J, Niemeier A
BONE. 2010;47(4):736-745.
Hypertriglyceridemia in obese subjects: caused by reduced apolipoprotein A5 plasma levels?
Heeren J, Merkel M
ATHEROSCLEROSIS. 2010;212(2):386-387.
Sort1, encoded by the cardiovascular risk locus 1p13.3, is a regulator of hepatic lipoprotein export.
Kjolby M, Andersen O, Breiderhoff T, Fjorback A, Pedersen K, Madsen P, Jansen P, Heeren J, Willnow T, Nykjaer A
CELL METAB. 2010;12(3):213-223.
Phosphorylation of sterol regulatory element-binding protein (SREBP)-1a links growth hormone action to lipid metabolism in hepatocytes.
Kotzka J, Knebel B, Avci H, Jacob S, Nitzgen U, Jockenhovel F, Heeren J, Haas J, Muller-Wieland D
ATHEROSCLEROSIS. 2010;213(1):156-165.
Genetic variation at chromosome 1p13.3 affects sortilin mRNA expression, cellular LDL-uptake and serum LDL levels which translates to the risk of coronary artery disease.
Linsel-Nitschke P, Heeren J, Aherrahrou Z, Bruse P, Gieger C, Illig T, Prokisch H, Heim K, Doering A, Peters A, Meitinger T, Wichmann H, Hinney A, Reinehr T, Roth C, Ortlepp J, Soufi M, Sattler A, Schaefer J, Stark K, Hengstenberg C, Schaefer A, Schreiber S, Kronenberg F, Samani N, Schunkert H, Erdmann J
ATHEROSCLEROSIS. 2010;208(1):183-189.
European Lipoprotein Club: report of the 31st ELC Annual Conference, Tutzing, 8-11 September 2008.
Bernini F, Freeman D, Groen A, Heeren J, Kalopissis A, Kronenberg F, Lindstedt K, Parini P, Schuster G, Anne T, Dij v, Willems K, von Eckardstein A
ATHEROSCLEROSIS. 2009;205(1):41-47.
Real-time magnetic resonance imaging and quantification of lipoprotein metabolism in vivo using nanocrystals.
Bruns O, Ittrich H, Peldschus K, Kaul M, Tromsdorf U, Lauterwasser J, Nikolic M, Mollwitz B, Merkel M, Bigall N, Sapra S, Reimer R, Hohenberg H, Weller H, Eychmüller A, Adam G, Beisiegel U, Heeren J
NAT NANOTECHNOL. 2009;4(3):193-201.
Receptor-Mediated Endocytosis and Intracellular Trafficking of Lipoproteins
Heeren J, Beisiegel U
2009. Cellular Lipid Metabolism. Springer Verlag Berlin Heidelberg: 213-237.
Insulin stimulates hepatic low density lipoprotein receptor-related protein 1 (LRP1) to increase postprandial lipoprotein clearance.
Laatsch A, Merkel M, Talmud P, Grewal T, Beisiegel U, Heeren J
ATHEROSCLEROSIS. 2009;204(1):105-111.
Effects of six APOA5 variants, identified in patients with severe hypertriglyceridemia, on in vitro lipoprotein lipase activity and receptor binding.
Dorfmeister B, Zeng W, Dichlberger A, Nilsson S, Schaap F, Hubacek J, Merkel M, Cooper J, Lookene A, Putt W, Whittall R, Lee P, Lins L, Delsaux N, Nierman M, Kuivenhoven J, Kastelein J, Vrablik M, Olivecrona G, Schneider W, Heeren J, Humphries S, Talmud P
ARTERIOSCL THROM VAS. 2008;28(10):1866-1871.
Duck hepatitis B virus requires cholesterol for endosomal escape during virus entry.
Funk A, Mouna M, Hohenberg H, Heeren J, Reimer R, Lambert C, Prange R, Sirma H
J VIROL. 2008;82(21):10532-10542.
European Lipoprotein Club: Report of the 30th ELC annual conference, Tutzing, 3-6 September 2007.
Hofker M, Bernini F, von Eckardstein A, Freeman D, Heeren J, Karpe F, Kalopissis A, Kronenberg F, Kuipers F, Lindstedt K, Parini P, Schuster G, Dijk v, Willems K
ATHEROSCLEROSIS. 2008;197(1):471-479.
Apoprotein A-V: An important regulator of triglyceride metabolism
Kluger M, Heeren J, Merkel M
J INHERIT METAB DIS. 2008;31(2):281-8.
Uptake of postprandial lipoproteins into bone in vivo: impact on osteoblast function.
Niemeier A, Niedzielska D, Secer R, Schilling A, Merkel M, Enrich C, Rensen P, Heeren J
BONE. 2008;43(2):230-237.
Characterization of lipid metabolism in insulin-sensitive adipocytes differentiated from immortalized human mesenchymal stem cells.
Prawitt J, Niemeier A, Kassem M, Beisiegel U, Heeren J
EXP CELL RES. 2008;314(4):814-824.
Recycling of apolipoprotein E is not associated with cholesterol efflux in neuronal cells.
Rellin L, Heeren J, Beisiegel U
BBA-MOL CELL BIOL L. 2008;1781(5):232-238.
Liver TAG transiently decreases while PL n-3 and n-6 fatty acids are persistently elevated in insulin resistant mice.
Scheja L, Tödter K, Mohr R, Niederfellner G, Michael M, Meissner A, Schoettler A, Pospisil H, Beisiegel U, Heeren J
LIPIDS. 2008;43(11):1039-1051.
Lipoprotein lipase-facilitated uptake of LDL is mediated by the LDL receptor.
Loeffler B, Heeren J, Blaeser M, Radner H, Kayser D, Aydin B, Merkel M
J LIPID RES. 2007;48(2):288-298.
Letzte Aktualisierung aus dem FIS: 28.05.2026 - 00:34 Uhr