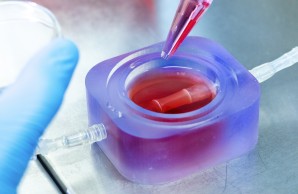
Pulsierendes Gewebe
Eine Herzkammer aus dem Reagenzglas, 1,8 cm klein, mit hauchdünnen Wänden. Das Gewebe, das in dem Bioreaktor gezüchtet wurde, pocht und leitet elektrische Signale weiter. In einigen Jahren soll daraus eine Herzkammer für Neugeborene werden. Priv.-Doz. Dr. Daniel Biermann und sein Team erläutern die Zusammenhänge.
Eine Herzkammer aus dem Labor
Organe züchten, um Leben zu retten: Das ist mehr als eine Vision. Wissenschaftler:innen des UKE haben aus Stammzellen ein erstes primitives Herz gezüchtet, das aussieht wie ein Schlauch und bereits rhythmisch schlägt. Es soll Säuglingen mit einem halben Herzen ein langes Leben schenken.
Von Silvia Dahlkamp, Fotos: Axel Kirchhof
Die siebte Schwangerschaftswoche. Auf dem Ultraschallbild erscheint ein Embryo. Gerade mal sieben Millimeter groß, doch in der Mitte flackert bereits ein winziger Punkt: das Herz. Zwei Kammern (Ventrikel), zwei Vorhöfe (Atrien), vier Klappen – alles ist angelegt. Ein Wunderwerk der Natur. Doch leider ist die Natur nicht perfekt. Bei einem von hundert Neugeborenen arbeitet das Herz nicht so, wie es soll. Und bei rund zwei Prozent der herzkranken Babys kommt es zu einem schwerwiegenden Defekt, dem Hypoplastischen Linksherzsyndrom – den Säuglingen fehlt ein halbes Herz. „Unser Körper kann vieles selbst reparieren, aber keine fehlenden Organe ersetzen. Da müssen wir helfen“, sagt Kinderherzchirurg Priv.-Doz. Dr. Daniel Biermann.
Beim hypoplastischen Linksherzsyndrom handelt es sich um eine der schwersten angeborenen Herzerkrankungen. Die unterentwickelte linke Herzkammer kann vorgeburtlich mittels Ultraschall diagnostiziert und meist erfolgreich operativ behandelt werden. „Die Behandlung beruht auf einer mehrstufigen operativen Strategie: von der ersten rekonstruktiven Operation in den ersten Lebenstagen über die zweite hämodynamische Anpassungsoperation im Säuglingsalter bis zur Trennung des Lungen- und Körperkreislaufs im Kleinkindalter. Durch dieses komplexe Verfahren können wir vielen Neugeborenen ein Überleben ermöglichen. Die langfristige Versorgung dieser Kinder erfordert aber eine kontinuierliche Betreuung durch interdisziplinäre Teams der Kinderherzmedizin, um ihre Stabilität und Lebensqualität nachhaltig zu sichern“, erklärt Prof. Dr. Michael Hübler, Direktor der Klinik und Poliklinik für Kinderherzmedizin und Erwachsene mit angeborenen Herzfehlern.
Was wäre, wenn das Implantat nicht aus Kunststoff, sondern aus humanem Gewebe bestünde, das wie ein Herz pumpen und mitwachsen kann? Diese Vorstellung ist inzwischen mehr als eine Vision. Nach intensiven Forschungen ist es einem Team aus Mediziner:innen, Biolog:innen und Techniker:innen am UKE gelungen, einen Tunnel aus menschlichen Herzmuskelzellen zu züchten, der pocht und selbst leichte elektrische Signale weiterleitet. Tissue Engineering heißt das Fachgebiet, Gewebezüchtung. Die Kammer aus dem Reagenzglas ist erst 1,8 Zentimeter klein, ihre Wände sind hauchdünn. Doch Dr. Biermann, stellvertretender Direktor der Klinik und Poliklinik für Kinderherzmedizin und Erwachsene mit angeborenen Herzfehlern, ist zuversichtlich: „In fünf Jahren wollen wir mit ersten klinischen Versuchen starten.“ Bis dahin soll aus dem zarten Gewebe ein starker Muskel werden.



Das Team arbeitet mit sogenannten induzierten pluripotenten Stammzellen (iPS-Zellen), die ursprünglich aus einer Hautbiopsie stammen und durch einen Virus umprogrammiert wurden. Pluripotente Stammzellen können jede Art von Baustein bilden – je nachdem, welcher Zelltyp wo im Organismus benötigt wird. Um die Zellen zu expandieren und die Zellteilung anzukurbeln, füttern die Forschenden zunächst einzelne iPS-Zellen mit bestimmten Nährmedien. In weniger als einer Woche entstehen so Millionen Zellkopien. Nach einer Differenzierungs- und Spezifizierungsphase fangen ab Tag sieben erste Zellanhäufungen spontan an zu schlagen, ziehen sich zusammen und strecken sich wieder. Was in einer Zellkulturflasche wie eine rot-orange, leicht trübe Flüssigkeit aussieht, sind unter dem Mikroskop tausende Zellen in kleinen Häufchen mit einem Durchmesser von weniger als einem halben Millimeter.
Welche Botenstoffe geben welcher Zelle wann den Impuls, sich in die eine oder andere Richtung zu entwickeln? Welche Reize beeinflussen das Wachstum? Wie bilden sich Gefäße, die das Zellgewebe durchbluten? Um die mikroskopisch kleine, aber trotzdem riesige Welt der Zellen besser zu verstehen, laufen im von Prof. Dr. Thomas Eschenhagen geleiteten Institut für Experimentelle Pharmakologie und Toxikologie rund um die Uhr Dutzende Experimente. Ziel ist es, einen biologischen Gewebetunnel zu schaffen, der das Blut effizient und mit dem richtigen Druck in den Lungenkreislauf pumpt. Dazu braucht es Ausdauer, Geduld – und extrem viele Zellen.
Doch wie verwandeln sich die Zellhäufchen in eine schlagende Herzkammer? „Es gibt ein strenges Protokoll“, sagt Ida Hüners, ebenfalls Assistenzärztinin der Kinderherzmedizin. Sie beobachtet und pflegt die Zellen, die bei 37 Grad Celsius in Inkubatoren leben. Nach 14 bis 18 Tagen findet der letzte Schritt, die Trennung der Zellhäufchen, statt. Die dabei gewonnenen Herzmuskelzellen werden mit verschiedenen Komponenten vermischt, unter anderem mit Thrombin, das den letzten Schritt der Blutgerinnungskaskade einleitet. „Es ist ein bisschen wie das strikte Befolgen eines Kochrezepts“, erklärt Hüners. Mit einer Pipette füllen die Forscher:innen den „Mastermix“ in eine selbstgebaute Gussform, die wie ein Infusionsschlauch aussieht und aus einem Innen- und Außenröhrchen aus Silikon besteht. Der Hohlraum dazwischen ist der Raum für die künstliche Herzkammer. Der Bioreaktor, in dem die Herzkammer sich entwickelt, wird mit Hilfe eines 3D-Druckers geschaffen. Läuft alles nach Plan, haben sich die Herzmuskelzellen nach 30 Minuten zwischen den Röhrchen verbunden und fangen nun an, sich umzubauen sowie zu reifen. Ein weiterer Schritt zum großen Ziel: Kranken Babys eine neue Herzkammer und ein normales Leben zu schenken.
Tissue Engineering
lautet der Oberbegriff für die Züchtung von menschlichen Zellen im Labor, an deren Entwicklung Prof. Dr. Thomas Eschenhagen, Direktor des Instituts für Experimentelle Pharmakologie und Toxikologie, maßgeblich mitgewirkt hat. Gemeinsam mit Kollegen aus den USA entwickelte er 1994 ein Verfahren zur Herstellung dreidimensionaler, künstlicher Herzgewebe. So ist es gelungen, mitwachsende Herzklappenprothesen für Kinder zu züchten. Getestet werden aktuell sogenannte Herzpflaster – im Labor gezüchtetes Gewebe aus kontrahierenden Muskelzellen. Bei Infarktpatient:innen wird eine Art Pflaster auf die Herzoberfläche genäht, das anwachsen und neues Gewebe bilden soll. Die Forschenden hoffen, die Herzfunktion auf diese Weise zu verbessern.
Auf diesen Forschungsseiten gibt es mehr Details:
www.uke.de/herzkammer