Cerebral Vasculitis Research
Die Cerebral Vasculitis Research group (CVR) beschäftigt sich in erster Linie mit der Verbesserung der Diagnostik der Primären Zerebralen Vaskulitis (Primary Angiitis of the central nervous system, PACNS).
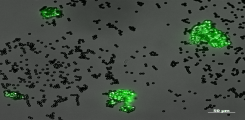
Die klinische Symptomatik ist wenig spezifisch. Auch die Untersuchungsbefunde, die im Rahmen der PACNS erhoben werden, sind durch eine geringe Spezifität gekennzeichnet. Die einzige Möglichkeit der Diagnosesicherung liegt in der Hirnbiopsie, welche jedoch häufig falsch-negative Befunde liefert. Hierdurch ergeben sich in der klinischen Praxis neben bioptisch-gesicherten, auch eine große Anzahl an PACNS-verdächtigen Fällen, in denen eine Sicherung der Diagnose nicht möglich ist.
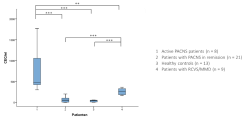
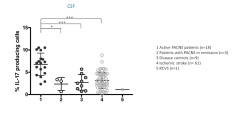
Die Hauptkompetenz unserer Arbeitsgruppe liegt in der Identifizierung neuer Biomarker bei der PACNS aus dem Blut und Nervenwasser (Liquor). Unser langfristiges Ziel ist, eine Reihe an Biomarkern (Biomarker-Panel) zu etablieren, die die Diagnostik der PACNS zukünftig verbessern können und somit vor allem in Patienten mit Verdacht auf eine PACNS die Sicherheit der Diagnose unterstützen. Auch sollen diese Marker dazu dienen, die Aktivität bzw. Akuität der Erkrankung anzuzeigen und auf diese Weise auch den Therapieerfolg zu überprüfen.
Darüber hinaus nehmen wir an dem prospektiven, multizentrischen, internationalen Vaskulitis-Register (German Vasculitis Registry, GeVas) teil und übernehmen hier die führende Koordination im Bereich der ZNS-Vaskulitis. Wir haben zudem eine Datenbank etabliert, die ausschließlich PACNS-Patienten mit histologischer Sicherung einschließt, um zukünftig mehr von Patienten mit gesicherter Diagnose lernen zu können.