 Startseite des UKE?
Startseite des UKE?

Determinanten der heterospezifischen Phasentrennung bei -ssRNA-Viren
Übersicht
Negativstrang-RNA-Viren (NSVs) replizieren sich innerhalb von Zellen in speziellen Strukturen, die als Einschlusskörper (IBs) bezeichnet werden. Dabei handelt es sich um membranlose Kompartimente, die aus viralen und Wirtsmolekülen gebildet werden, häufig durch einen Prozess, der als Flüssig-Flüssig-Phasentrennung (LLPS) bekannt ist. Obwohl viele Proteine das Potenzial haben, solche Strukturen zu bilden, ist noch unklar, warum nur bestimmte Proteine in virale IBs rekrutiert werden – und welche Rolle das virale Genom in diesem Prozess spielt. Unser Ziel ist es, die zugrunde liegenden Regeln aufzudecken, die die Bildung dieser viralen Kompartimente steuern. Das Verständnis dieser Prinzipien könnte uns helfen, neue Inhibitoren zu entwickeln, die sowohl gegen bekannte Viren als auch gegen zukünftige Bedrohungen wie „Krankheit X“ eingesetzt werden können.
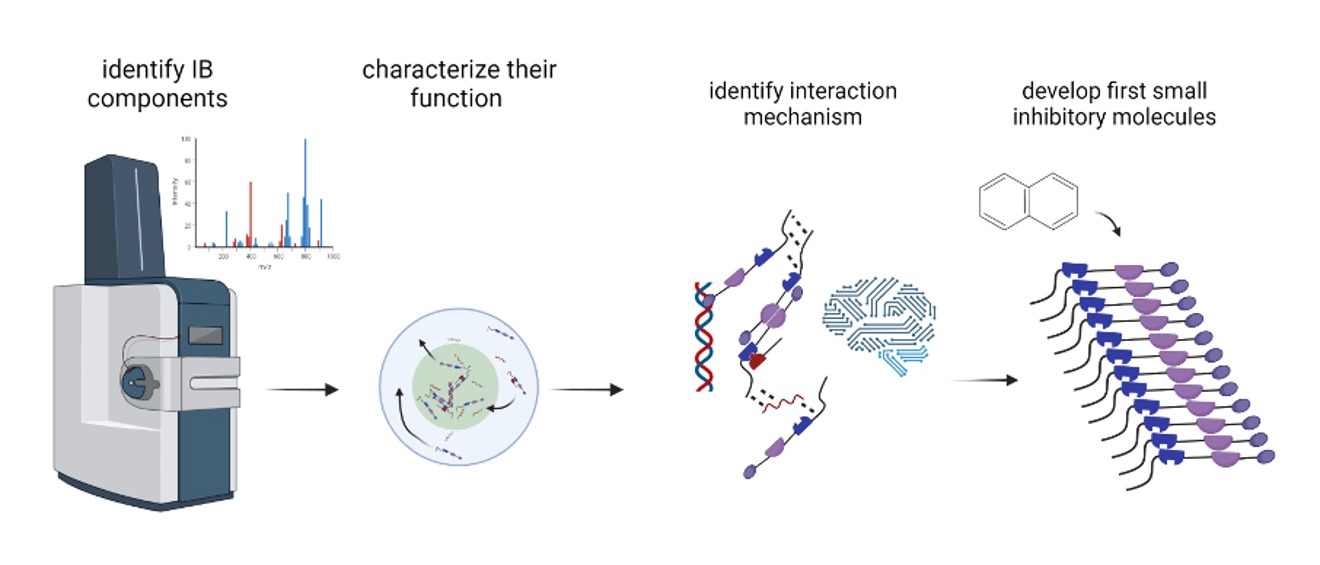
Unsere Arbeitspakete (engl.: Work packages, WP):
WP1: Ermöglichung der Klick-Markierung viraler RNA in lebenden Zellen mithilfe der TriPPPro-Technologie – Wir entwickeln eine neue Markierungsmethode, um virale RNA in lebenden Zellen sichtbar zu machen und zu verfolgen, wo und wann sie während der Infektion mit anderen Molekülen interagiert.
WP2: Identifizierung von Proteinen in genomassoziierten Einschlusskörpern – Wir identifizieren, welche zellulären und viralen Proteine in viralen Einschlusskörpern vorhanden sind, und untersuchen, wie sie mit viraler RNA und Replikation in Verbindung stehen.
WP3: Entschlüsselung des Mechanismus der Rekrutierung in phasengetrennte Einschlusskörper – Wir untersuchen, wie bestimmte Proteine selektiv in Einschlusskörper rekrutiert werden und welche Teile ihrer Struktur dies ermöglichen.
WP4: Entwicklung von IB-spezifischen Inhibitoren durch gezielte Beeinflussung kondensatspezifischer Wechselwirkungen – Wir nutzen die Erkenntnisse aus WP1–3, um kleine Moleküle zu entwickeln, die virale Einschlusskörper zerstören oder stabilisieren und die Virusvermehrung blockieren.
Diese Arbeitspakete helfen uns zu verstehen, wie virale Einschlusskörper (IBs) entstehen und funktionieren – und wie wir sie gezielt bekämpfen können, um die Ausbreitung gefährlicher Viren zu stoppen.
Das Team


Prof. Dr. Chris Meier
Projektleiter
E-Mail:
Telefon: +49 40 42838-4324


Prof. Dr. Jens Bosse
Projektleiter
E-Mail:
Telefon: +49 040 8998 87645





Forschungsgruppe Meier
Die Forschungsgruppe Synthetische Organische Chemie, Medizinische Chemie und Chemische Biologie ist an der Universität Hamburg angesiedelt.
Forschungsgruppe Bosse
Die Forschungsgruppe Quantitative Virology ist am Centre for Structural Systems Biology (CSSB) angesiedelt.
Projektbezogene Publikationen
Sterrenberg VT#, Stalling D#, Knaack JIH, Soh TK, Bosse JB#, Meier C#. A TriPPPro-Nucleotide Reporter with Optimized Cell-Permeable Dyes for Metabolic Labeling of Cellular and Viral DNA in Living Cells. Angew Chem Int Ed Engl. 2023;62(38):e202308271. doi: 10.1002/anie.202308271.
Caragliano E, Bonazza S, Frascaroli G, …, Grünewald K, Bosse JB#, Brune W#. Human cytomegalovirus forms phase-separated compartments at viral genomes to facilitate viral replication. Cell Rep. 2022;38(10):110469. doi: 10.1016/j.celrep.2022.110469.
Zhao C, Jia X, Schols D, Balzarini J, Meier C. gamma-Non-Symmetrically Dimasked TriPPPro Prodrugs as Potential Antiviral Agents against HIV. ChemMedChem. 2021;16(3):499–512. doi: 10.1002/cmdc.202000712.
Jung J, Ching W, Baumdick M, …, Bosse JB, …, Belderbos M, Dobner T, Bunders M. KIR3DS1 directs NK cell-mediated protection against human adenovirus infections. Sci Immunol. 2021;6(63):eabe2942. doi: 10.1126/sciimmunol.abe2942.
Jia X, Weber S, Schols D, Balzarini J, Meier C. Membrane Permeable, Bioreversibly Modified Prodrugs of Nucleoside Diphosphate-γ-Phosphonates. J Med Chem. 2020;63(20):11990–12007. doi: 10.1021/acs.jmedchem.0c01294.
Zhao C, Weber S, Schols D, …, Balzarini J, Meier C. Prodrugs of γ-Alkyl-Modified Nucleoside Triphosphates: Improved Inhibition of HIV Reverse Transcriptase. Angew Chem Int Ed Engl. 2020;59(49):22063–22071. doi: 10.1002/anie.202003073.
Gollnest T, Dinis de Oliveira T, Rath AK, …, Schols D, Balzarini J, Meier C. Membrane-permeable Triphosphate Prodrugs of Nucleoside Analogues. Angew Chem Int Ed Engl. 2016;55(17):5255–5258. doi: 10.1002/anie.201511808.
Gollnest T, Dinis de Oliveira T, Schols D, Balzarini J, Meier C. Lipophilic prodrugs of nucleoside triphosphates as biochemical probes and potential antivirals. Nat Commun. 2015;6:8716. doi: 10.1038/ncomms9716.
Bosse JB, Hogue IB, Feric M, …, Sodeik B, Brangwynne CP, Enquist LW. Remodeling nuclear architecture allows efficient transport of herpesvirus capsids by diffusion. Proc Natl Acad Sci U S A. 2015;112(42):E5725–E5733. doi: 10.1073/pnas.1513876112.
Hagen C#, Dent KC#, Zeev-Ben-Mordehai T#, Grange M#, Bosse JB#, …, Plitzko JM, Mettenleiter TC, Grünewald K. Structural Basis of Vesicle Formation at the Inner Nuclear Membrane. Cell. 2015;163(7):1692–1701. doi: 10.1016/j.cell.2015.11.029.
#equally contributing authors