 Startseite des UKE?
Startseite des UKE?

Strukturelle Zellbiologie von Bunyaviren
Übersicht
Bunyaviren sind weltweit verbreitet und können eine Vielzahl von Organismen infizieren. Einige Mitglieder dieser Virusfamilie, wie das Lassa-Virus (LASV) und das Rift-Valley-Fieber-Virus (RVFV), sind für wiederkehrende Ausbrüche verantwortlich und gelten als ernsthafte Bedrohung für die öffentliche Gesundheit, was durch ihre Aufnahme in die R&D Blueprint-Liste der WHO bestätigt wird. Trotzdem ist die Biologie der Bunyaviren nach wie vor kaum verstanden. Diese Viren bestehen aus kleinen, membrangebundenen Partikeln und benötigen nur eine minimale Anzahl von viralen Proteinen – die oft multifunktional sind –, um ihren Lebenszyklus zu vollenden. Ein wichtiges Beispiel ist das L-Protein, ein großes und komplexes Enzym, das für die Kopie und Transkription des viralen Genoms verantwortlich ist.
Obwohl einige strukturelle Details des L-Proteins bereits bekannt sind, gibt es noch viele offene Fragen darüber, wie die Genomreplikation und Transkription in infizierten Zellen abläuft und welche Faktoren des Wirts und des Virus dabei eine Rolle spielen. Dieses Projekt zielt darauf ab, diese Wissenslücken zu schließen, indem untersucht wird, wie die Replikations- und Transkriptionsprozesse innerhalb der Zellen organisiert sind, vom Eindringen des Virus bis zu seiner Assemblierung. Mithilfe fortschrittlicher Bildgebungstechniken wie der Kryo-Elektronentomographie (cryoET) und der Einzelpartikel-Kryo-Elektronenmikroskopie (cryoEM) hoffen die Forscher, wichtige molekulare Wechselwirkungen aufzudecken, die als neue Ziele für die Entwicklung antiviraler Medikamente dienen könnten.
Unsere Arbeitspakete (engl.: Work packages, WP):
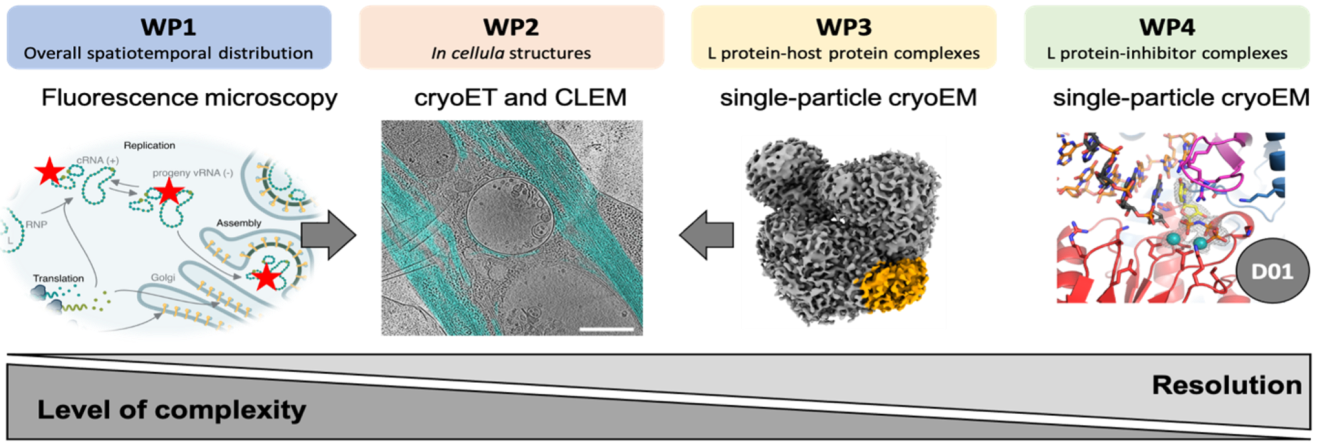
Dieses Projekt besteht aus vier miteinander verbundenen Arbeitspaketen, die darauf abzielen, den Lebenszyklus des Bunyavirus auf verschiedenen Detailebenen aufzudecken – von der räumlichen Lokalisierung innerhalb von Zellen bis hin zu hochauflösenden Strukturanalysen.
WP1: Visualisierung der Virusreplikation in Raum und Zeit – Wir untersuchen mithilfe modernster Fluoreszenzmikroskopie, wo und wann das L-Protein von LASV und RVFV die virale Transkription und Replikation in Wirtszellen durchführt.
WP2: Strukturelle Einblicke in virale Prozesse in Zellen – wir verwenden Kryo-Elektronentomographie (KryoET) und korrelative Mikroskopie, um zu visualisieren, wie Bunyaviren während des Eindringens, der Replikation und des Austritts zelluläre Strukturen umformen.
WP3: Hochauflösende Strukturen viraler Polymerase-Wirt-Interaktionen – wir bestimmen die 3D-Strukturen des L-Proteins im Komplex mit Wirtsfaktoren und RNA mithilfe von Einzelpartikel-Kryo-EM, um die Wechselwirkungen zwischen Wirt und Virus auf atomarer Ebene zu verstehen.
WP4: Strukturelle Grundlage der Hemmung des L-Proteins – Wir bewerten die Wirkung von Nukleotidhemmern auf das L-Protein mithilfe biochemischer Assays und hochauflösender Kryo-EM, um die Optimierung antiviraler Wirkstoffe zu steuern.
Diese Arbeitspakete helfen uns dabei, die Virusreplikation, die Wechselwirkungen mit dem Wirt und die Wirkungen von Inhibitoren systematisch zu analysieren und liefern damit die strukturelle und funktionelle Grundlage für zukünftige therapeutische Strategien.
Das Team


Prof. Dr. Kay Grünewald
Projektleiter
E-Mail:
Telefon: +49 40 8998 87700


Dr. Maria Rosenthal
Projektleiterin
E-Mail:
Telefon: +49 40 285380-930




Forschungsgruppe Grünewald
Die Abteilung Structural Cell Biology of Viruses ist am Centre for Structural Systems Biology (CSSB) angesiedelt.
Forschungsgruppe Rosenthal
Die Forschungsgruppe Strukturelle Virologie ist am Bernhard-Nocht-Institut für Tropenmedizin (BNITM) angesiedelt.
Projektbezogene Publikationen
Williams HM, Thorkelsson SR, Vogel D, Milewski M, Busch C, Cusack S, Grünewald K, Quemin ERJ, Rosenthal M. Structural insights into viral genome replication by the severe fever with thrombocytopenia syndrome virus L protein. Nucleic Acids Res. 2023;51(3):1424–1442. doi: 10.1093/nar/gkac1249.
Kouba T#, Vogel D#, Thorkelsson SR#, Quemin ERJ, Williams HM, Milewski M, Busch C, Günther S, Grünewald K, Rosenthal M, Cusack S. Conformational changes in Lassa virus L protein associated with promoter binding and RNA synthesis activity. Nat Commun. 2021;12(1):7018. doi: 10.1038/s41467-021-27305-5.
Vogel D, Rosenthal M, Gogrefe N, Reindl S, Günther S. Biochemical characterization of the Lassa virus L protein. J Biol Chem. 2019;294(20):8088. doi: 10.1074/jbc.RA118.006973.
Jérôme H, Rudolf M, Lelke M, Pahlmann M, Busch C, Bockholt S, Wurr S, Günther S, Rosenthal M, Kerber R. Rift Valley fever virus minigenome system for investigating the role of L protein residues in viral transcription and replication. J Gen Virol. 2019;100(7):1093–1098. doi: 10.1099/jgv.0.001281.
Moser F#, Pražák V#, Mordhorst V, Andrade DM, Baker LA, Hagen C, Grünewald K, Kaufmann R. Cryo-SOFI enabling low-dose super-resolution correlative light and electron cryo-microscopy. PNAS. 2019;116(11):4804–4809. doi: 10.1073/pnas.1810690116.
Hagen C#, Dent KC#, Zeev-Ben-Mordehai T#, Grange M#, Bosse JB#, Whittle C, Klupp BG, Siebert CA, Vasishtan D, Bäuerlein FJB, Cheleski J, Werner S, Guttman P, Rehbein S, Henzler K, Demmerle J, Adler B, Koszinowski U, Schermelleh L, Schneider G, Enquist LW, Plitzko JM, Mettenleiter TC, Grünewald K. Structural Basis of Vesicle Formation at the Inner Nuclear Membrane. Cell. 2015;163(7):1692–1701. doi: 10.1016/j.cell.2015.11.029.
Schellenberger P, Kaufmann R, Siebert CA, Hagen C, Wodrich H, Grünewald K. High-precision correlative fluorescence and electron cryo microscopy using two independent alignment markers. Ultramicroscopy. 2014;143(100):41–51. doi: 10.1016/j.ultramic.2013.10.011.
Huiskonen JT, Hepojoki J, Laurinmäki P, Vaheri A, Lankinen H, Butcher SJ, Grünewald K. Electron cryotomography of Tula hantavirus suggests a unique assembly paradigm for enveloped viruses. J Virol. 2010;84(10):4889–4897. doi: 10.1128/JVI.00057-10.
Huiskonen JT, Overby AK, Weber F, Grünewald K. Electron cryo-microscopy and single-particle averaging of Rift Valley fever virus: evidence for GN-GC glycoprotein heterodimers. J Virol. 2009;83(8):3762–3769. doi: 10.1128/JVI.02483-08.
#equally contributing authors