Mucolipidose Typ II und III
Co-Projektleitung: Sandra Pohl
- Forschung
- Team
- Publikationen
- Förderung
- Links
-
Forschung
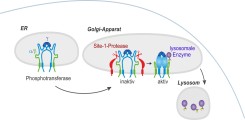
Der Phosphotransferase-Komplex generiert Mannose-6-Phosphat-Signale, die für den effizienten Transport lysosomalen Enzyme zu den Lysosomen benötigt werden. Mutationen in den Genen, die die Untereinheiten der Phosphotransferase kodieren, führen zu den lysosomalen Speicherkrankheiten Mucolipidose Typ II und III. Biochemisch führt das Fehlen von Mannose-6-Phosphat-Signalen zur Fehlsortierung lysosomaler Enzyme und zur Speicherung von nicht abbaubaren Makromolekülen in den Lysosomen. Wir untersuchen die Bedeutung einzelner Domänen für die Interaktionen der Untereinheiten und der Funktion der Phosphotransferase, sowie Regulationsprozesse des Transports der Phosphotransferase vom endoplasmatischen Retikulum (ER) zum Golgi-Apparat und der proteolytischen Aktivierung durch die Site-1-Protease. Die Daten werden neue Einsichten in regulatorische proteolytische Ereignisse und Netzwerke geben, die für die Funktion von Lysosomen wichtig sind.
-
Team
Co-Projektleitung
 Prof. Dr. rer. nat.Sandra PohlTelefonE-Mail
Prof. Dr. rer. nat.Sandra PohlTelefonE-MailPostdoctoral Fellows
 Dr. rer. nat.Tatyana DanyukovaTelefonE-Mail
Dr. rer. nat.Tatyana DanyukovaTelefonE-MailDoktoranden
 Lena WestermannTelefon
Lena WestermannTelefonTechnische Assistenz
Ehemalige Mitarbeiter
Giorgia Di Lorenzo, PhD
Dr. rer. nat. Raffaella De Pace
Dr. rer. nat. Sarah Klünder
Dr. rer. nat. Marisa Encarnação
Dr. rer. nat. Katrin Marschner
Dr. med. Luce Laverne Darnell
Dr. med. Bastian ThiesAngelika Mojzisch, MSc
Lisa-Marie Böttcher, BSc
Estelle Domo, BSc
Saskia Grüb, MSc
Sophia Klause, MSc
Dipl. Biol. Lola Rozikova
Julia Schimanowski, BSc
-
Publikationen
Projektrelevante Publikationen
- Subunit interactions of the disease-related hexameric GlcNAc-1-phosphotransferase complex. De Pace R, Velho RV, Encarnação M, Marschner K, Braulke T, Pohl S (2015) Hum Mol Genet 24:6826-35 Abstract
- Site-1 protease-activated formation of lysosomal targeting motifs is independent of the lipogenic transcription control. Klünder S, Heeren J, Markmann S, Santer R, Braulke T, Pohl S (2015) J Lipid Res 56:1625-1632 Abstract
- Analyses of disease-related GNPTAB mutations define a novel GlcNAc-1-phosphotransferase interaction domain and an alternative site-1 protease cleavage site. Velho RV, De Pace R, Klünder S, Sperb-Ludwig F, Lourenço CM, Schwartz IV, Braulke T, Pohl S (2015) Hum Mol Genet 24:3497-3505 Abstract
- A key enzyme in the biogenesis of lysosomes is a protease that regulates cholesterol metabolism. Marschner K, Kollmann K, Schweizer M, Braulke T, Pohl S (2011) Science 333:87-90 Abstract
- Posttranslational modifications of the γ-subunit affect intracellular trafficking and complex assembly of the GlcNAc-1-phosphotransferase. Encarnação M, Kollmann K, Trusch M. Braulke T, Pohl S (2011) J Biol Chem 286: 5311-18 Abstract
- Proteolytic processing of the γ-subunit is associated with the failure to form GlcNAc-1-phosphotransferase complexes and mannose 6-phosphate residues on lysosomal enzymes in human macrophages. Pohl S, Tiede S, Marschner K, Encarnação M, Castrichini M, Kollmann K, Muschol N, Ullrich K, Müller-Loennies S, Braulke T (2010) J Biol Chem 285:23936-44 Abstract
- Mucolipidosis II is caused by mutations in GNPTA encoding the alpha/beta GlcNAc-1-phosphotransferase. Tiede S, Storch S, Lübke T, Henrissat B, Bargal R, Raas-Rothschild A, Braulke T (2005) Nat Med 11:1109-12 Abstract
-
Förderung
Laufende Förderung

04/2018 - 03/2021
Sandra Pohl
Deutsche Forschungsgemeinschaft
Grant PO 1539/1-1
„Role of the gamma-subunit of the GlcNAc-1-phosphotransferase complex for selective mannose 6-phosphate modifications on lysosomal enzymes“
07/2010 - 06/2022
Sandra Pohl & Thomas Braulke
Deutsche Forschungsgemeinschaft
Sonderforschungsbereich 877:
"Proteolysis as a Regulatory Event in Pathophysiology"
www.uni-kiel.de/Biochemie/sfb877/Abgeschlossene Förderung

03/2017 - 02/2018
Sandra Pohl
ISMRD - International Society for Mannosidosis & Related Diseases (USA)
"Osteoporosis in Mucolipidosis II - A potential corrective approach"
http://www.ismrd.org/research
05/2008 - 04/2017
Thomas Braulke (Sprecher + Koordination),
Sandra Pohl & Stephan Storch
Deutsche Forschungsgemeinschaft
Graduiertenkolleg 1459:
"Sortierung und Wechselwirkungen zwischen
Proteinen subzellulärer Kompartimente"
www.grk1459.de -
-
Links